
| A. | 为减小酸碱中和滴定的使用误差,锥形瓶必须洗净、烘干后使用 | |
| B. | 在氨水中加入少量的水或氯化铵固体后,都会使溶液中的c(H+)增大 | |
| C. | 已知NaAlO2溶液的pH>7,将其蒸干并灼烧后得到的残留物为NaAlO2 | |
| D. | 由H+(aq)+OH-(aq)=H2O(I)△H=-57.3kJ•mol-1,可知100mL 0.1mol•L-1的氨水混合,放出的热量等于0.573kJ |
分析 A.锥形瓶无需干燥;
B.加水稀释促进一水合氨电离,加入氯化铵固体抑制一水合氨电离;
C.NaAlO2溶液加热生成氢氧化铝和氢氧化钠,最终仍生成NaAlO2;
D.一水合氨为弱电解质,电离吸热.
解答 解:A.锥形瓶无论是否干燥,对实验结果都没有影响,故A错误;
B.加水稀释促进一水合氨电离,一水合氨电离增大程度小于溶液体积增大程度,所以溶液中c(OH-)减小,加入氯化铵固体抑制一水合氨电离,一水合氨电离向逆反应方向移动,导致溶液中c(OH-)减小,c(H+)增大,故B正确;
C.NaAlO2溶液加热生成氢氧化铝和氢氧化钠,最终仍生成NaAlO2,故C正确;
D.一水合氨为弱电解质,电离吸热,则100 mL 0.1 mol•L-1 的盐酸与100 mL 0.1 mol•L-1 的氨水混合,放出的热量小于0.573 kJ,故D错误.
故选BC.
点评 本题考查较为综合,涉及中和滴定、弱电解质的电离、盐类的水解等问题,侧重于学生的分析能力的考查,题目难度不大,注意盐类水解的原理,特别是能把握相关物质的性质.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
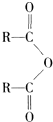 $\stackrel{H_{2}O}{→}$2RCOOH ②RCOOH$\stackrel{LiAlH_{4}}{→}$RCH2OH
$\stackrel{H_{2}O}{→}$2RCOOH ②RCOOH$\stackrel{LiAlH_{4}}{→}$RCH2OH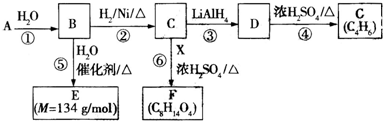
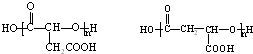 (一种即可).
(一种即可).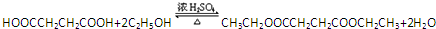 .
. .Y与足量氢氧化钠溶液反应所得产物之一M,能与灼热的氧化铜反应,写出M与灼热的氧化铜反应的化学方程式:
.Y与足量氢氧化钠溶液反应所得产物之一M,能与灼热的氧化铜反应,写出M与灼热的氧化铜反应的化学方程式: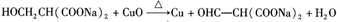 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 在氨水中加入少量的水或氯化铵固体后,都能使溶液中的c(NH4+)减小 | |
| B. | 相同体积、pH均为3的HA和HB两种酸分别与足量的锌充分反应,HA放出的氢气多,说明HB的酸性比HA的酸性强 | |
| C. | 工业电解食盐水中,电解池被阳离子交换膜隔成阴极室和阳极室,目的是避免阳极产生的气体与烧碱反应 | |
| D. | 在等浓度的NaCl和Na2CrO4稀溶液中滴加AgNO3溶液,先析出AgCl沉淀,则Ksp(AgCl)<Ksp(Ag2CrO4) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
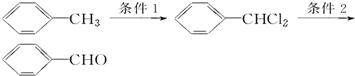
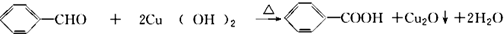 .
.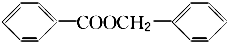 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
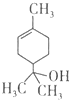
| A. | 1mol该物质最多能和lmol氢气发生加成反应 | |
| B. | 该物质属于烃 | |
| C. | 该物质能使溴水褪色 | |
| D. | 分子式为C9H16O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na、Al、Fe、Cu在空气中都易生锈是因为都生成了对应的氧化物 | |
| B. | 在高温下用氢气还原MgCl2可制取金属镁 | |
| C. | 实验测得NH4HCO3溶液显碱性,CH3COONH4溶液显中性,说明酸性CH3COOH>H2CO3 | |
| D. | 高温时,CuO比Cu2O稳定,Na2O2比Na2O稳定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com