
(12分)N2(g)+3H2(g)  2NH3(g)反应过程的能量变化如下图所示。
2NH3(g)反应过程的能量变化如下图所示。

已知生成1 mol NH3(g)的ΔH=-46 kJ·mol-1。请回答下列问题:
(1)图中A、C分别表示 、 ;若该反应使用催化剂,会使图中B点升高还是降低? 。
(2)图中ΔH= kJ·mol-1。
(3)已知恒容时,该体系中各物质浓度随时间变化的曲线如图所示。

①在0.5 L容器中发生反应,前20 min内,v(NH3)=________,放出的热量为________。
②45 min时采取的措施是_______________________。
③比较I、II、III时段的化学平衡常数(分别用K1、K2、K3表示)大小________。
21.(1)反应物总能量; 生成物总能量; 降低;(每空各1分) (2)-92
(3)①0.050 mol/(L·min) (1分); 23.6 Kj ②降低体系温度 ③K3>K1=K2
【解析】
试题分析:(1)由图可知,图中A、B分别表示反应物总能量;生成物总能量,催化剂降低反应的活化能,所以若该反应使用催化剂,会使图中B点降低;(2)因为生成1 mol NH3(g)的ΔH=-46 kJ·mol-1,则N2(g)+3H2(g)  2NH3(g),ΔH=-92 kJ·mol-1,所以反应过程的能量变化ΔH=-92kJ·mol-1;
2NH3(g),ΔH=-92 kJ·mol-1,所以反应过程的能量变化ΔH=-92kJ·mol-1;
(3)①读图可知,前20min内氨气的浓度由0逐渐增大到1.0mol/L,根据定义式可得,v(NH3)=1.0mol/L÷20min=0.050mol/(L?min);氮气由1.0mol/L逐渐减小到0.50mol/L,根据c?V=n可求参加反应的氮气的物质的量,即(1.0—0.50)mol/L?0.5L=0.25mol,由于N2(g)+3H2(g) 2NH3(g) △H=-94.4kJ·mol-1表示1mol氮气反应放出94.4kJ热量,放出的热量为94.4x0.25=23.6kJ热量;②读图可知,45min时氨气的浓度平缓上升,氮气和氢气的浓度则平缓下降,采取的措施是降低体系温度,平衡向正反应方向移动,则氮气、氢气的浓度均减小,氨气的浓度逐渐增大;③时段I和时段II温度不变,K1=K2,时段III降低温度,K值增大,所以K3>K1=K2。
2NH3(g) △H=-94.4kJ·mol-1表示1mol氮气反应放出94.4kJ热量,放出的热量为94.4x0.25=23.6kJ热量;②读图可知,45min时氨气的浓度平缓上升,氮气和氢气的浓度则平缓下降,采取的措施是降低体系温度,平衡向正反应方向移动,则氮气、氢气的浓度均减小,氨气的浓度逐渐增大;③时段I和时段II温度不变,K1=K2,时段III降低温度,K值增大,所以K3>K1=K2。
考点:考查反应热,化学反应原理。


科目:高中化学 来源:2014-2015学年重庆市高二上学期9月培优复习化学试卷(解析版) 题型:实验题
用浓度为0.10 mol/L的KMnO4(H+)溶液滴定未知浓度的H2C2O4(弱酸)溶液,其实验步骤如下:
I、滴定前的准备:
① → 用蒸馏水清洗 → 用待装溶液润洗 → 装液→ ② → 调节液面在零刻度或零刻度以下 → 记录初始读数
II、滴定:
分别取20.00 mL 草酸溶液于4个洁净的锥形瓶中,滴加几滴MnSO4溶液,然后用标准的KMnO4(H+)溶液进行滴定至终点,记录最终读数。数据如下:
测定次序 | 第一次 | 第二次 | 第三次 | 第四次 |
初始读数(mL) | 0.40 | 0.10 | 0.90 | 0.00 |
最终读数(mL) | 25.05 | 20.10 | 21.00 | 19.90 |
V标(mL) | 24.65 | 20.00 | 20.10 | 19.90 |
III、实验数据处理:略
请回答下列问题:
(1)将步骤I中的操作补充完整:
①__________________________ ②__________________________
(2)KMnO4(H+)溶液应装入________式滴定管进行滴定;
(3)向锥形瓶中滴加MnSO4溶液的作用是_____________________________________;判断已达滴定终点的现象是:_____________________________________;
(4)该滴定反应的离子方程式为:__________________________________________;
(5)实验测得草酸溶液的浓度为_____________mol/L;
(6)下列操作会引起实验结果偏高的是_____________
A.向锥形瓶中加入了较多 MnSO4溶液
B.滴定振摇时,锥形瓶中溶液溅出
C.滴定时,锥形瓶内壁附有紫红色溶液,未用蒸馏水冲洗
D.滴定结束时,仰视读数
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁省高二上学期10月月考化学试卷(解析版) 题型:选择题
某烯烃与氢气加成后得到2,2-二甲基丁烷,该烃的名称是( )
A.3,3,3-三甲基-1-丁炔 B.2,2-二甲基-2-丁烯
C.2,2-二甲基-1-丁烯 D.3,3-二甲基-1-丁烯
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁省高一上学期10月月考化学试卷(解析版) 题型:选择题
下列有关实验操作或判断正确的是
A.配制一定物质的量浓度的溶液,定容时俯视刻度线会导致所配溶液浓度偏小
B.需要95 mL 0.1 mol·L-1NaCl溶液,可选用100 mL容量瓶来配制
C.用100 mL的量筒量取5.2 mL的盐酸
D.用托盘天平称取25.20 g NaCl
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁省五校协作体高二上学期期中化学试卷(解析版) 题型:选择题
一定温度下,将1molM和1molN气体充入2L恒容密闭容器,发生反应M(g)+ N(g) xP(g)+Q(s),t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中气体P的浓度随时间变化如图所示。
xP(g)+Q(s),t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中气体P的浓度随时间变化如图所示。
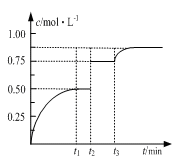
下列说法正确的是
A.反应方程式中的x=1
B.t2时刻改变的条件是使用催化剂
C.t3时刻改变的条件是移去少量物质Q
D.t1~t3间该反应的平衡常数均为4
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁省五校协作体高二上学期期中化学试卷(解析版) 题型:选择题
下列与化学反应能量变化相关的叙述正确的是
A.2CH3CH2OH(l)+6O2(g)===4CO2(g)+6H2O(l) ΔH=-1367kJ/mol,可见乙醇燃烧热ΔH=-1367 kJ/mol
B.放热反应的反应速率总是大于吸热反应的反应速率
C.应用盖斯定律,可计算某些难以直接测量的反应焓变
D.同温同压下,H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件下的ΔH不同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com