
 +4H+=2
+4H+=2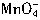 +MnO2+2H2O,但最高产率只有66.7%,所以制取KMnO4常用电解法,即以铁和石墨做电极电解K2MnO4溶液,下列有关叙述正确的是( )。
+MnO2+2H2O,但最高产率只有66.7%,所以制取KMnO4常用电解法,即以铁和石墨做电极电解K2MnO4溶液,下列有关叙述正确的是( )。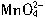 →
→ +e-
+e-科目:高中化学 来源: 题型:阅读理解
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:2013-2014学年湖北省孝感市高三第二次统考理综化学试卷(解析版) 题型:填空题
MnO2、KMnO4等是中学化学中的常用试剂。请回答下列问题:
(1)MnO2在H2O2分解反应中作催化剂。若将MnO2加入酸化的H2O2溶液中,MnO2 溶解产生Mn2+,反应的离子方程式是??????????????????????????????????????????????? 。
(2)用MnO2制KMnO4的工艺流程如图
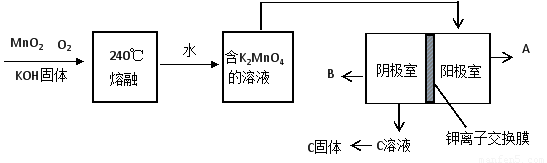
电解池中两极材料均为碳棒,在水或酸性溶液中K2MnO4发生歧化而变成MnO2和KMnO4。
①写出240℃熔融时发生反应的化学方程式????????????????????????????????????? ,投料时必须满足n(KOH):n(MnO2) ?????????? 。
②阳极的电极反应为??????????????????????????????????? 。
③B物质是????????? (写化学式,下同),可以循环使用的物质是???????????????????? 。
④钾离子交换膜的一种材料是聚丙烯酸钾(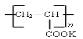 ),聚丙烯酸钾单体的结构简式为??????????? 。
),聚丙烯酸钾单体的结构简式为??????????? 。
⑤上述制得的KMnO4产品0.165 g,恰好与0.335 g经硫酸酸化的Na2C2O4反应完全,该KMnO4的
纯度是??????????? (精确到0.1%)。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年上海市高三上学期第三次月考化学试卷(解析版) 题型:填空题
许多物质的氧化能力受溶液酸碱性的影响。高锰酸钾在不同的条件下发生的还原反应如下:
MnO4—+ 5e + 8H+ → Mn2+ + 4H2O
MnO4— + 3e + 2H2O → MnO2 + 4OH—
MnO4— + e → MnO42—(溶液呈绿色)
MnO2的还原反应可表示如下:MnO2+4H+ + 2e → Mn2++2H2O
(1)MnO2 与稀盐酸不能制取氯气,其原因是 。
(2)将SO2通入KMnO4溶液中,发生还原反应的过程为______→_______
(用化学式或离子符号表示)。
(3)将PbO2投入到酸性MnSO4溶液中搅拌,溶液变为紫红色。下列叙述正确的是________(选填编号)。
a.氧化性:PbO2>KMnO4 b.还原性:PbO2> KMnO4
c.该反应可以用盐酸酸化
(4)将高锰酸钾溶液逐滴加入到硫化钾溶液中可发生如下反应,其中K2SO4和S的物质的量之比为3:2。完成并配平该反应的化学方程式。
___KMnO4+___K2S+___ _____ → ___K2MnO4 +___K2SO4 +__S↓+___ ___
反应若生成5.44 g单质硫,反应过程中转移电子的物质的量为__________。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年广西桂林十八中高三(上)第三次月考化学试卷(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com