
分析 锌比铜活泼,形成原电池反应时,锌为负极,发生氧化反应,电极反应式为Zn-2e-=Zn2+,铜为正极,发生还原反应,电极反应式为2H++2e-=H2↑,结合原电池工作原理及电极反应式进行相关的计算.
解答 解:锌比铜活泼,形成原电池反应时,锌为负极,发生氧化反应,电极反应式为Zn-2e-=Zn2+,铜为正极,发生还原反应,电极反应式为2H++2e-=H2↑,锌片的质量减少了6.5克,n(Zn)=$\frac{6.5g}{65g/mol}$=0.1mol,铜表面析出了氢气为0.1mol×22.4L/mol=2.24L,导线上通过0.2mol电子时,SO42-向负极移动,氢离子浓度减小,则溶液的pH值增大;用离子方程式表示电极的总反应式为Zn+2H+=Zn2++H2↑,
故答案为:2.24;0.2;负极;增大;2H++2e-=H2↑;Zn+2H+=Zn2++H2↑.
点评 本题考查原电池知识,为高考常见题型,侧重于学生的分析能力和计算能力的考查,注意把握电极反应式的书写,题目难度不大.


科目:高中化学 来源: 题型:解答题
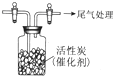 某学习小组推测SO2能与强氧化剂Cl2反应生成SO2Cl2,为此进行探究.
某学习小组推测SO2能与强氧化剂Cl2反应生成SO2Cl2,为此进行探究.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化碳的电子式: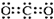 | B. | 14C的原子结构示意图: | ||
| C. | C3H8的结构式CH3-CH2-CH3 | D. | 次氯酸的电子式: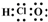 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 C的离子结构示意图:
C的离子结构示意图: .
.
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 反应:L(s)+aG(g)?bR(g) 达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数.
反应:L(s)+aG(g)?bR(g) 达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数.| A. | a<b | B. | 上述反应是吸热反应 | ||
| C. | a>b | D. | 上述反应是放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
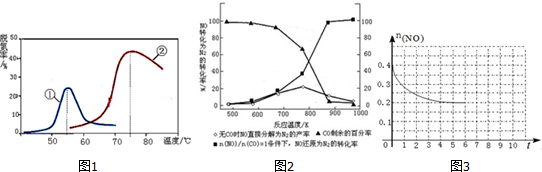
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
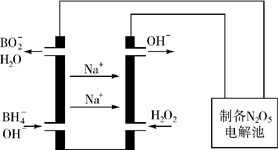 氮的重要化合物如氨、肼(N2H4)、NO、NO2、HNO3、硝酸盐等,在生产、生活中具有重要作用.
氮的重要化合物如氨、肼(N2H4)、NO、NO2、HNO3、硝酸盐等,在生产、生活中具有重要作用.| 0.01mol•L-1的溶液 | X | Y | Z | W |
| pH | 12 | 2 | 8.5 | 4.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 晶体硅常用作半导体材料 | B. | 二氧化硅不能与任何酸反应 | ||
| C. | 硅在地壳中主要以化合态形式存在 | D. | 硅酸可通过硅酸钠与盐酸反应制得 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 比较去锈的铁钉和去锈的绕有细铜丝的铁钉与同浓度的盐酸反应速率快慢时,可以加K3[Fe(CN)6]溶液,观察铁钉周围出现蓝色沉淀的快慢 | |
| B. | 将在空气中灼烧呈黑色的铜丝趁热插入盛有乙醇的试管中,铜丝变红色;反复数次,试管中的液体出现刺激性气味,表明乙醇已被铜氧化为乙醛 | |
| C. | 欲粗略测定某未知浓度的醋酸溶液中醋酸的电离常数Ka,应做的实验和所需的试剂(或试纸)为:中和滴定实验、pH试纸 | |
| D. | 从海带中提取碘,可将灰化后的海带加入水中煮沸一段时间后过滤,向滤液中滴入几滴硫酸,再加入适量H2O2溶液氧化,最后加入CCl4萃取分离 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com