
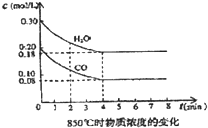
 ��һ���Ϊ10L�������У�ͨ��һ������CO��H2O����85��ʱ�������·�Ӧ��CO��g��+H2O��g��?CO2��g��+H2��g����H=-Q kJ/mol CO��H2OŨ�ȱ仯��ͼ����
��һ���Ϊ10L�������У�ͨ��һ������CO��H2O����85��ʱ�������·�Ӧ��CO��g��+H2O��g��?CO2��g��+H2��g����H=-Q kJ/mol CO��H2OŨ�ȱ仯��ͼ����| ʱ�� | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | C1 | C2 | C3 | C3 |
| 4 | C1 | C2 | C3 | C3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
| ��C |
| ��t |
| ��C |
| ��t |
| (0.20-0.08)mol/L |
| 4min |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
 ��֪��Ӧ��CO��g��+H2O��g��?H2��g��+CO2��g����H=-41.2kJ/mol�����ɵ�CO2��H2�Բ�ͬ������Ȼ��ʱ�ں��������µķ�Ӧ���Ƶ�CH4��
��֪��Ӧ��CO��g��+H2O��g��?H2��g��+CO2��g����H=-41.2kJ/mol�����ɵ�CO2��H2�Բ�ͬ������Ȼ��ʱ�ں��������µķ�Ӧ���Ƶ�CH4��| 1 | 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��12�֣�ij���淴Ӧ��ƽ�ⳣ������ʽ ������ʱ���¶�����H2Ũ�ȼ�С���Իش��������⣺
��1���÷�Ӧ�Ļ�ѧ����ʽΪ�� ��
��2���¶����ߣ��÷�Ӧ��Kֵ______________(�������С�����䡱)����ѧƽ���ƶ��ﵽ�µ�ƽ���CO2��CO�����___________(�������С�����䡱)��
��3����һ���Ϊ10L�������У�ͨ��һ������CO��H2O����850��ʱ������Ӧ��CO��H2OŨ�ȱ仯����ͼ���� 0��4min��ƽ����Ӧ����v(CO)��___________mol��(L��min)��850��Ļ�ѧƽ�ⳣ����ֵK=
��4��850��ʱ������ͬ�����з�����ӦCO2+ H2 CO+H2O (g)��tʱ�������ڸ����ʵ�Ũ�ȷֱ�Ϊ��һ����̼0.09 mol��L��ˮ����0.09mol��L�� ������̼0.08 mol��L������ 0.08 mol��L����ʱv(��) v(��)�������ڡ��� С�ڡ����ڡ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010�꽭��ʡ�Ž�һ�и߶���ѧ�ڵ�һ���¿�����ѧ�� ���ͣ������
��12�֣�ij��Ӧ��ƽ�ⳣ������ʽΪ ������ʱ���¶�����.H2Ũ�ȼ�С�������������⣺
������ʱ���¶�����.H2Ũ�ȼ�С�������������⣺
��1���÷�Ӧ�Ļ�ѧ����ʽΪ��
��2���¶����ߣ��÷�Ӧ��Kֵ______________(�������С�����䡱)����ѧƽ���ƶ���ﵽ�µ�ƽ�⣬CO2��CO�����_______________(�������С�����䡱)��
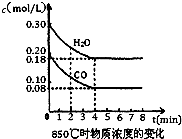
��3����һ���Ϊ10L�������У�ͨ��һ������CO��H2O����850��ʱ������Ӧ��CO��H2OŨ�ȱ仯����ͼ���� 0��4min��ƽ����Ӧ����v(CO)��______ mol��(L��min)��850��Ļ�ѧƽ�ⳣ����ֵK= 
��4��850��ʱ������ͬ�����з�����ӦCO2+ H2 CO+H2O (g)��tʱ�������ڸ����ʵ�Ũ�ȷֱ�Ϊ��һ����̼0.09 mol��L��ˮ����0.09 mol��L��������̼0.08 mol��L������ 0.08 mol��L����ʱv(��) v(��)�������ڡ��� С�ڡ������ڡ���
CO+H2O (g)��tʱ�������ڸ����ʵ�Ũ�ȷֱ�Ϊ��һ����̼0.09 mol��L��ˮ����0.09 mol��L��������̼0.08 mol��L������ 0.08 mol��L����ʱv(��) v(��)�������ڡ��� С�ڡ������ڡ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ��ɽ��ʡ�������и߶���ѧ������ѧ���϶���ѧ�Ծ� ���ͣ������
��12�֣�ij���淴Ӧ��ƽ�ⳣ������ʽ ������ʱ���¶�����H2Ũ�ȼ�С���Իش�
������ʱ���¶�����H2Ũ�ȼ�С���Իش� �������⣺
�������⣺
��1���÷�Ӧ�Ļ�ѧ����ʽΪ��  ��
��
��2���¶����ߣ��÷�Ӧ��Kֵ______________(�������С�����䡱)����ѧƽ���ƶ��ﵽ�µ�ƽ���CO2��CO�����___________(�������С�����䡱)��
��3����һ���Ϊ10L�������У�ͨ��һ������CO��H2O����850��ʱ������Ӧ��CO��H2OŨ�ȱ仯����ͼ���� 0��4min��ƽ����Ӧ����v(CO)��___________ mol��(L��min)��850��Ļ�ѧƽ�� ������ֵK=
������ֵK= 
��4��850��ʱ������ͬ�����з�����ӦCO2+ H2 CO+H2O (g)��tʱ�������ڸ����ʵ�Ũ�ȷֱ�Ϊ��һ����̼0.09 mol��L��ˮ����0.09 mol��L�� ������̼0.08 mol��L������ 0.08
CO+H2O (g)��tʱ�������ڸ����ʵ�Ũ�ȷֱ�Ϊ��һ����̼0.09 mol��L��ˮ����0.09 mol��L�� ������̼0.08 mol��L������ 0.08 mol��L����ʱv(��) v(��)�������ڡ��� С�ڡ����ڡ���
mol��L����ʱv(��) v(��)�������ڡ��� С�ڡ����ڡ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013��ɽ��ʡ�������и߶���ѧ������ѧ���϶���ѧ�Ծ� ���ͣ������
��12�֣�ij���淴Ӧ��ƽ�ⳣ������ʽ ������ʱ���¶�����H2Ũ�ȼ�С���Իش��������⣺
������ʱ���¶�����H2Ũ�ȼ�С���Իش��������⣺
��1���÷�Ӧ�Ļ�ѧ����ʽΪ�� ��
��2���¶����ߣ��÷�Ӧ��Kֵ______________(�������С�����䡱)����ѧƽ���ƶ��ﵽ�µ�ƽ���CO2��CO�����___________(�������С�����䡱)��
��3����һ���Ϊ10L�������У�ͨ��һ������CO��H2O����850��ʱ������Ӧ��CO��H2OŨ�ȱ仯����ͼ���� 0��4min��ƽ����Ӧ����v(CO)��___________ mol��(L��min)��850��Ļ�ѧƽ�ⳣ����ֵK=

��4��850��ʱ������ͬ�����з�����ӦCO2+ H2  CO+H2O (g)��tʱ�������ڸ����ʵ�Ũ�ȷֱ�Ϊ��һ����̼0.09 mol��L��ˮ����0.09
mol��L�� ������̼0.08 mol��L������ 0.08 mol��L����ʱv(��)
v(��)�������ڡ��� С�ڡ����ڡ���
CO+H2O (g)��tʱ�������ڸ����ʵ�Ũ�ȷֱ�Ϊ��һ����̼0.09 mol��L��ˮ����0.09
mol��L�� ������̼0.08 mol��L������ 0.08 mol��L����ʱv(��)
v(��)�������ڡ��� С�ڡ����ڡ���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com