
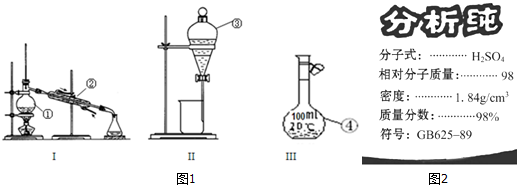
分析 (1)熟悉仪器构造,说出其名称;
(2)能用来盛放液体,且有活塞的仪器使用时必须检查是否漏水;分离溴水中的溴应先加入萃取剂,使溶液分层,然后用分液漏斗进行分液操作分离;
(3)①依据配制一定物质的量浓度溶液的一般步骤选择仪器解答;
②依据C=$\frac{1000ρω}{M}$计算浓硫酸的物质的量浓度,依据溶液稀释过程中溶质的物质的量不变计算需要浓硫酸体积;
③分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析.
解答 解;(1)图中①为蒸馏烧瓶;②为冷凝管;
故答案为:①蒸馏烧瓶;②冷凝管;
(2)分液漏斗、容量瓶都能用来盛放液体,且有活塞,使用时必须检查是否漏水;分离溴水中的溴应先加入萃取剂,使溶液分层,然后用分液漏斗进行分液操作分离;
故答案为:3、4,II;
(3)①用浓硫酸配制一定浓度的稀硫酸,步骤为:计算、量取、稀释、移液、洗涤、定容,用到的仪器:量筒、烧杯、玻璃棒、容量瓶、胶头滴管,除量筒、烧杯、玻璃棒、胶头滴管等外,此实验还需要的主要仪器250mL容量瓶,上图中没有;
故答案为:无;250ml容量瓶;
②浓硫酸物质的量浓度C=$\frac{1000×1.84×98%}{98}$=18.4mol/L,配制浓度为0.18mol•L-1的稀硫酸210mL,应选择250mL容量瓶,设需要浓硫酸体积为V,则依据溶液稀释过程中溶质的物质的量不变得:18.4mol/L×V=0.18mol/L×250mL,解得V=2.4mL;
故答案为:2.4;
③A.用相同装置配制过0.10mol/L的硫酸溶液后,未清洗即,进行此实验的配制,量取的硫酸的物质的量偏大,溶液浓度偏高,故A选;
B.移液时未对烧杯和玻璃棒进行洗涤,导致部分溶质损耗,溶质的物质的量偏小,溶液浓度偏低,故B不选;
C.定容时仰视刻度线,导致溶液体积偏大,溶液浓度偏低,故C不选;
D.颠倒摇匀后发现液面低于刻度线,但未加水至刻度线,属于正常操作,对溶质的物质的量和溶液体积都不会产生影响,溶液浓度准确,故D不选;
故选:A.
点评 本题为实验题,考查了常见仪器的名称和使用注意事项,一定物质的量浓度溶液的配制,侧重考查学生对基本实验掌握的熟练程度,题目难度不大.


 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4LH2O所含电子数为10NA | |
| B. | 0.1mol/LBa(OH)2溶液中含有0.2NA个OH- | |
| C. | 0.5molNH4HSO4晶体中,含有H+数目约为0.5NA | |
| D. | 常温常压下,3.2gO3混合气体含有0.2NA个氧原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡是单质参加的化合反应都是氧化还原反应 | |
| B. | 碱性氧化物均是金属氧化物 | |
| C. | 金属单质在参加的反应中只能作还原剂 | |
| D. | 非金属单质在参加的反应中只能作氧化剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com