
| 元素编号 | 元素特征信息 |
| A | 其单质是密度最小的物质 |
| B | 其阴离子带两个单位负电荷,单质是空气的主要成分之一 |
| C | 其阳离子与B的阴离子有相同的电子层结构,且与B可以形成两种离子化合物 |
| D | 其氢氧化物和氧化物都有两性,与C同周期 |
| E | 与C同周期,原子半径在该周期最小 |
分析 A、B、C、D、E五种短周期主族元素,A的单质是密度最小的物质,则A为H元素;B的阴离子带两个单位负电荷,单质是空气的主要成分之一,则B为O元素;C的阳离子与B的阴离子有相同的电子层结构,且与B可以形成两种离子化合物,则C为Na;D的氢氧化物和氧化物都有两性,且与C同周期,则D为Al;E与C同周期,原子半径在该周期最小,则E为Cl.
解答 解:A、B、C、D、E五种短周期主族元素,A的单质是密度最小的物质,则A为H元素;B的阴离子带两个单位负电荷,单质是空气的主要成分之一,则B为O元素;C的阳离子与B的阴离子有相同的电子层结构,且与B可以形成两种离子化合物,则C为Na;D的氢氧化物和氧化物都有两性,且与C同周期,则D为Al;E与C同周期,原子半径在该周期最小,则E为Cl.
(1)C单质与水反应的化学方程式为:2Na+2H2O=2NaOH+H2↑,
故答案为:2Na+2H2O=2NaOH+H2↑;
(2)工业制取D单质的化学方程式为:2Al 2O3$\frac{\underline{\;通电\;}}{\;}$4Al+3O2↑,
故答案为:2Al 2O3$\frac{\underline{\;通电\;}}{\;}$4Al+3O2↑;
(3)D单质为Al,C的最高价氧化物对应的水化物为NaOH,二者反应的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(4)实验室制取氯气的离子方程式为:MnO2+4 H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,
故答案为:MnO2+4 H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O.
点评 本题考查结构性质位置关系应用,侧重对化学用语的考查,熟练掌握元素化合物性质,比较基础.


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 酸性:HIO4>HBrO4>HClO4 | B. | 原子半径:Na>Cl>S | ||
| C. | 碱性:KOH>NaOH>LiOH | D. | 金属性:Na>Al>Mg |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
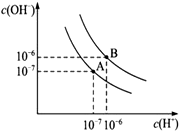 已知水在25℃和95℃时,其电离平衡曲线如图所示:
已知水在25℃和95℃时,其电离平衡曲线如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
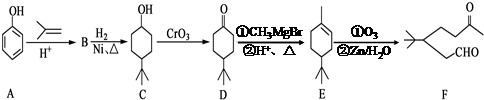
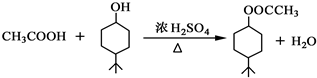 .
.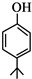 .同时满足下列条件的B的同分异构体(不包括B)共有11种:
.同时满足下列条件的B的同分异构体(不包括B)共有11种:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
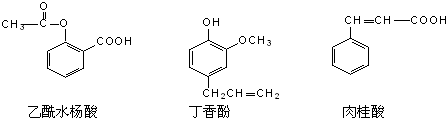
| A. | ①② | B. | ③④ | C. | ①③④ | D. | ①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka=3.0×10-8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
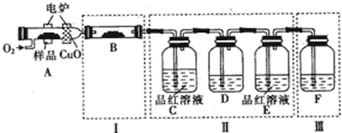
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2SO2+O2?2SO3 | B. | CO2+H2O?H2CO3 | C. | CO+H2O(g)?CO2+H2 | D. | H++OH-?H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com