
| 编号 | Cu | Zn | S |
| 1 | 10.3% | 5.0% | 1.2% |
| 2 | 11.5% | 4.9% | 1.8% |
| 3 | 12.4% | 10.3% | 0.9% |
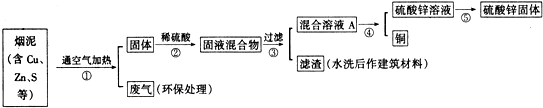
分析 煤泥中含有的硫能与空气中的氧气反应生成二氧化硫,能形成酸雨,通入空气后,铜会与氧气反应生成氧化铜,氧化铜能与硫酸反应生成硫酸铜和水,硫酸过量,加入的锌粉能与硫酸反应生成硫酸锌和氢气,硫酸铜能与锌反应生成硫酸锌和铜,
(1)步骤①②中含铜元素的物质为氧化铜,硫酸铜;氧化铜和硫酸反应;
(2)本方案中废气是由硫和氧气发生化学反应生成的二氧化硫,有效地吸收它,最好用氢氧化钠溶液;
(3)⑤步中由硫酸铜溶液,得到其固体,需要蒸发结晶;
(4)混合溶液A为:硫酸铜和硫酸锌,锌和硫酸铜反应生成硫酸锌和铜.
解答 解:煤泥中含有的硫能与空气中的氧气反应生成二氧化硫,能形成酸雨,通入空气后,铜会与氧气反应生成氧化铜,氧化铜能与硫酸反应生成硫酸铜和水,硫酸过量,加入的锌粉能与硫酸反应生成硫酸锌和氢气,硫酸铜能与锌反应生成硫酸锌和铜,
(1)步骤①②中含铜元素的物质为氧化铜,硫酸铜,与反应的化学方程式为2Cu+O2$\frac{\underline{\;加热\;}}{\;}$2CuO、CuO+H2SO4=CuSO4+H2O,
故答案为:2Cu+O2$\frac{\underline{\;加热\;}}{\;}$2CuO; CuO+H2SO4=CuSO4+H2O;
(2)本方案中废气是由硫和氧气发生化学反应生成的二氧化硫,有效地吸收它,最好用氢氧化钠溶液,反应的化学方程式为2NaOH+SO2=Na2SO3+H2O,
故答案为:2NaOH+SO2=Na2SO3+H2O;
(3)⑤步中由硫酸铜溶液,得到其固体,需要蒸发结晶,故答案为:蒸发结晶(或蒸发、浓缩、结晶);
(4)混合溶液A为:硫酸铜和硫酸锌,锌和硫酸铜反应生成硫酸锌和铜,故答案答为:Zn.
点评 本题考查物质的分离、提纯,为高频考点,侧重于学生的分析、实验能力的考查,注意把握物质的性质以及实验原理、操作的方法等知识,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9种 | B. | 8种 | C. | 6种 | D. | 4种 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
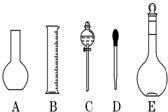 实验室需要0.1mol/L NaOH溶液450mL和0.5mol/L硫酸溶液450mL.根据这两种溶液的配制情况回答下列问题:
实验室需要0.1mol/L NaOH溶液450mL和0.5mol/L硫酸溶液450mL.根据这两种溶液的配制情况回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
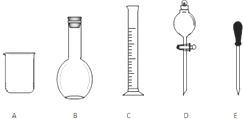 实验室需要0.1mol/L NaOH溶液480mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.
实验室需要0.1mol/L NaOH溶液480mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与氢氧化钠反应的氯气一定为0.16 mol | |
| B. | n(Na+):n(Cl-)可能为7:3 | |
| C. | 若反应中转移的电子为n mol,则0.15<n<0.25 | |
| D. | n(NaCl):n(NaClO):n(NaClO3)可能为11:2:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com