
某反应2AB(g) C(g)+ 3D (g)在高温下能自发进行,其逆反应在低温下能自发进行,
C(g)+ 3D (g)在高温下能自发进行,其逆反应在低温下能自发进行,
则该反应的Δ H、Δ
H、Δ S应为
S应为
A.ΔH <0,ΔS>0 B.ΔH <0,ΔS<0 C.ΔH >0,ΔS> 0 D.ΔH >0,ΔS<0
0 D.ΔH >0,ΔS<0
科目:高中化学 来源: 题型:
下列有关实验操作或结论的叙述中不正确的是( )
|
|
|
|
|
| A.除去CO2中的HCl | B.溶液变红,待测液中含Fe3+ | C.有砖红色沉淀,葡萄糖中含醛基 | D.有白烟出现,浓盐酸有挥发性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
重金属元素铬的毒性较大,含铬废水需经处理达标后才能排放。
Ⅰ.某工业废水中主要含有Cr3+,同时还含有少量的Fe3+、Al3+、Ca2+和Mg2+等,且酸性较强。为回收利用,通常采用如下流程处理:
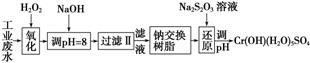
注:部分阳离子常温下以氢氧化物形式完全沉淀时溶液的pH见下表。
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 | Al(OH)3 | Cr(OH)3 |
| pH | 3.7 | 9.6 | 11.1 | 8 | 9(>9溶解) |
(1)氧化过程中可代替H2O2加入的试剂是________(填序号)。
A.Na2O2 B.HNO3 C.FeCl3 D.KMnO4
(2)加入NaOH溶液调整溶液pH=8时,除去的离子是________;已知钠离子交换树脂的原理:Mn++nNaR—→MRn+nNa+,此步操作被交换除去的杂质离子是__________。
A.Fe3+ B.Al3+ C.Ca2+ D.Mg2+
(3)还原过程中,每消耗0.8 mol Cr2O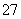 转移4.8 mol e-,该反应离子方程式为________________________________________________________________________。
转移4.8 mol e-,该反应离子方程式为________________________________________________________________________。
Ⅱ.酸性条件下,六价铬主要以Cr2O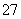 形式存在,工业上常用电解法处理含Cr2O
形式存在,工业上常用电解法处理含Cr2O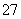 的废水:
的废水:
该法用Fe作电极电解含Cr2O 的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3溶液。
的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3溶液。
(1)电解时能否用Cu电极来代替Fe电极?________(填“能”或“不能”),理由是________________________________________________________________________。
(2)电解时阳极附近溶液中Cr2O 转化为Cr3+的离子方程式为__________________________
转化为Cr3+的离子方程式为__________________________
______________________________________________。
(3)常温下,Cr(OH)3的溶度积Ksp=1×10-32,溶液的pH应为________时才能使c(Cr3+)降至10-5 mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对实验操作或对实验事实的描述正确的是( )
A.用瓷坩埚熔化各种钠的化合物
B.向氨水中滴加Al2(SO4)3溶液和向Al2(SO4)3溶液中滴加氨水现象不同
C.配制一定浓度的溶液时,俯视容量瓶的刻线,会使配制的浓度偏低
D.实验室配制氯化亚铁溶液时,将氯化亚铁先溶解在稀盐酸中,然后用蒸馏水稀释并加入少量铁粉
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验方案或操作正确的是( )
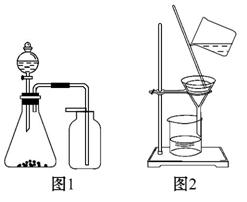
A.选择合适的试剂,用图1装置可分别制取和收集少量CO2、NO
B.除去石英(主要成分SiO2)中少量碳酸钙:用稀盐酸溶解后过滤
C.洗涤沉淀时(见图2),向漏斗中加适量水,搅拌并滤干
D.用广范pH试纸测得0.1 mol·L-1NH4Cl溶液pH=5.2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实中,不能用勒夏特列原理解释的是
A.盛有NO2和N2O4 混合气体的烧瓶置于热水中,气体颜色变深
B .工业合
.工业合 成氨选择500oC左右的
成氨选择500oC左右的 温度比室温有利
温度比室温有利
C.实验室中常用排饱和食盐水的方法收集Cl2
D.合成氨时采用循环操作及将氨液化分离,可提高原料的利用率
查看答案和解析>>
科目:高中化学 来源: 题型:
下列图示与对应的叙述相符的是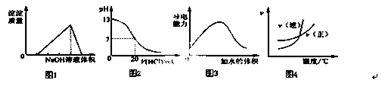
A.图1表示向某硫酸和硫酸铝混合溶液中加入NaOH溶液,沉淀质量与加入NaOH溶液体积的关系
B.图2表示25℃时,用0.1mol•L-1盐酸滴定20mL0.1mol•L-1NaOH溶液的pH随加 入盐酸体积的变化
入盐酸体积的变化 
C.图3表示t℃时稀释冰醋酸过程中溶液导电性的变化
D.根据图4可 判断某可逆反应的正反应是吸热反应
判断某可逆反应的正反应是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是实验室干馏煤的装置图,回答下列问题:
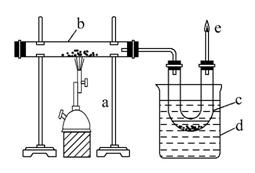
(1)指出图中仪器名称:
c ,d 。
(2)仪器d的作用是 ,
c中液体有 和 ,其中无机物里溶有 ,可用 检验出来。有机物可以通过 的方法使其中的重要成分分离出来。
(3)e处点燃的气体主要成分有 ,
火焰的颜色 。
查看答案和解析>>
科目:高中化学 来源: 题型:
为了将混有K2SO4、MgSO4的KNO3固体提纯,并制得纯净的KNO3溶液,某学生设计如下实验方案:
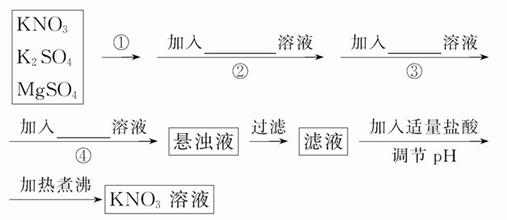
(1)操作①为 。
(2)操作②~④加入的试剂依次可以为:_________________________________。
(3)如何判断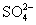 已除尽? ____________________________________________。
已除尽? ____________________________________________。
(4)实验过程中产生的多次沉淀__________(填“需要”或“不需要”)多次过滤,其理由是________________________________________________________。
(5)该同学的实验设计方案是否严密?请说明理由: _______________________
___________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com