
COCl2(g)CO(g)+Cl2(g) ΔH>0。当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是( )
A.①②④ B.①④⑥
C.②③⑥ D.③⑤⑥
科目:高中化学 来源: 题型:
我国“十一五”规划纲要提出,“十一五”期间单位国内生产总值能耗降低20%左右,主要污染物排放总量减少10%。日前召开的国务院常务会议进一步明确了节能减排的主要目标任务和总体要求。下列措施与节能减排不符合的是( )
A.利用太阳能制氢燃料
B.加大石油、煤炭的开采速度,增加化石燃料的供应量
C.利用潮汐能发电
D.大力开展农村沼气的普及
查看答案和解析>>
科目:高中化学 来源: 题型:
“西气东输”是我国开发的重点工程,这里的气是指天然气,其主要成分是甲烷。工业上将碳与水在高温下反应制得水煤气,水煤气的主要成分是CO和H2,二者的体积比为11。已知1 mol CO气体完全燃烧生成CO2气体放出282.6 kJ热量;1 mol氢气完全燃烧生成液态水放出285.8 kJ热量;1 mol CH4气体完全燃烧生成CO2气体和液态水放出889.6 kJ热量。
(1)写出氢气完全燃烧生成液态水的热化学方程式:
________________________________________________________________________________________________________________________________________________。
(2)若1 mol CH4气体完全燃烧生成CO2气体和水蒸气,放出的热量________(填“大于”“等于”或“小于”)889.6 kJ。
(3)忽略水煤气中其他成分,相同状况下若得到相等的热量,所需水煤气与甲烷的体积比约为(整数比)________。
(4)以上数据和计算说明,以天然气替代水煤气作燃料,突出的优点是____________________________________________________ ____________________________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,在密闭容器中能表示反应X(g)+2Y(g)2Z(g)一定达到平衡状态的是( )
①X、Y、Z的物质的量之比为1:2:2 ②X、Y、Z的浓度不再发生变化 ③容器中的压强不再发生变化 ④单位时间内生成n mol Z,同时生成2n mol Y
A.①② B.①④
C.②③ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
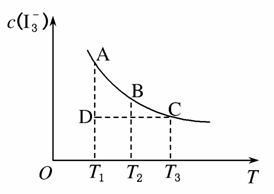
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)I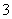 (aq),某I2、KI混合溶液中I
(aq),某I2、KI混合溶液中I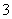 的物质的量浓度c(I
的物质的量浓度c(I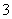 )与温度T的关系如图所示,(曲线上任何一点都表示平衡状态)。下列说法正确的是( )
)与温度T的关系如图所示,(曲线上任何一点都表示平衡状态)。下列说法正确的是( )
A.反应:I2(aq)+I-(aq)I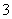 (aq)的ΔH>0
(aq)的ΔH>0
B.若温度为T1、T2,反应平衡常数分别为K1、K2,则K1<K2
C.若反应进行到状态D时,一定有ν正>ν逆
D.状态A与状态B比较,状态A的c(I2)大
查看答案和解析>>
科目:高中化学 来源: 题型:
在450 ℃并有催化剂存在下,于一容积恒定的密闭容器内进行下列反应:
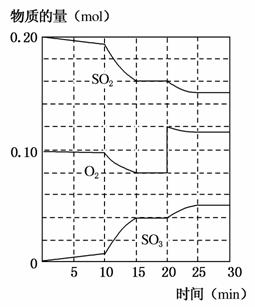
2SO2(g)+O2(g)2SO3(g) ΔH=-190 kJ·mol-1
(1)该反应500 ℃时的平衡常数________450 ℃时的平衡常数(填“>”、“<”或“=”)。
(2)450 ℃时,在一2 L密闭容器中,将二氧化硫和氧化混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态的时间是________________。
(3)据图判断,反应进行至20 min时,曲线发生变化的原因是__________________(用文字表达),10 min到15 min的曲线变化的原因可能是________(填字母)。
A.加了催化剂
B.缩小容器体积
C.降低温度
D.增加SO3物质的量
(4)欲提高SO2的转化率,下列措施可行的是________。(填字母)
a.向装置中再充入N2
b.向装置中再充入O2
c.改变反应的催化剂
d.升高温度
(5)利用图中数据计算450 ℃时反应进行至15 min时,SO2的平衡转化率为:________。
(6)450 ℃时,另一2 L容积不变的密闭容器中,测得某时刻各物质的量如下:
n(SO2)=0.4 mol,n(O2)=0.2 mol,n(SO3)=0.8 mol,则此时该反应向________进行(填“正反应方向”“逆反应方向”或“处于平衡状态”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.原子晶体中原子间以共价键相结合
B.稀有气体形成的晶体属于分子晶体
C.干冰升华时,分子内共价键会发生断裂
D.金属元素和非金属元素形成的化合物不一定是离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
下列图示与对应的叙述相符的是
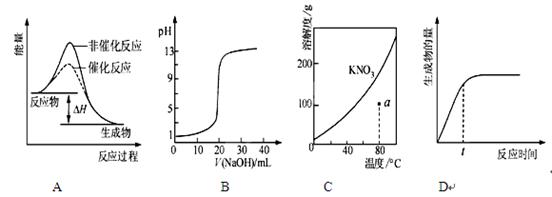
A.表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化
B.表示0.1000mol·L-1NaOH溶液滴定20.00mL 0.1000mol·L-1CH3COOH溶液所得到的滴定曲线
C.表示KNO3的溶解度曲线,图中a点所示的溶液是80 ℃时KNO3的不饱和溶液
D.表示某可逆反应生成物的量随反应时间变化的曲线,由图知t时反应物转化率最大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com