
| 危险性 | 危险品 |
| 储运要求 | 远离金属粉末、氨、烃类、醇等物质,设置氯气检测仪 |
| 泄漏处理 | NaOH、NaHSO3溶液吸收 |
| 包装 | 钢瓶 |
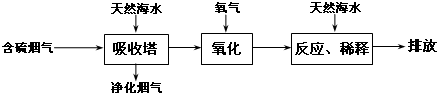
分析 (1)①将氯气液化,可降低温度或压强;
②NaHSO3溶液与泄露的氯气发生氧化还原反应;在钢瓶表面氯与苯的反应明显加快,催化剂加快反应速率;
(2)①SO2与过量海水中OH-发生复分解反应生成亚硫酸钠和水;
②H2SO3或HSO3-中的S显+4价,均可被O2氧化生成H++SO42-,酸性会大大增强,氧化后的“海水”需要引入大量的显碱性的海水与之混合后才能排放,主要目的是中和、稀释经氧气氧化后海水中生成的酸(H+);
(3)①工业上把海水先进行氧化,再吸收溴,达到富集溴的目的.吸收工艺常用的方法是用热空气吹出Br2;
②根据Br-和BrO3-在酸性条件下发生归中反应生成Br2,该反应中Br元素化合价由+5价、-1价变为0价,所以溴既是氧化产物也是还原产物,且有$\frac{1}{6}$的溴来自于BrO3-,据此计算.
解答 解:(1)常温下,氯气为气体,降温 (或加压)可液化,转化为液体便于运输和储存,
故答案为:降温 (或加压);
(3)①NaHSO3溶液与泄露的氯气发生氧化还原反应,离子反应为HSO3-+Cl2+H2O═SO42-+2Cl-+3H+,
故答案为:HSO3-+Cl2+H2O═SO42-+2Cl-+3H+;
②由在钢瓶表面氯与苯的反应明显加快可知,铁与氯气反应生成的氯化铁,对氯与苯的反应有催化作用,
故答案为:铁与氯气反应生成的氯化铁,对氯与苯的反应有催化作用;
(2)①SO2与过量海水中OH-发生复分解反应生成亚硫酸钠和水,离子反应为SO2+2OH-═SO32-+H2O,
故答案为:SO2+2OH-═SO32-+H2O;
②H2SO3或HSO3-中的S显+4价,均可被O2氧化生成H+和SO42-,酸性会大大增强,H2SO3被氧化的化学方程式为:2H2SO3+O2=2H2SO4,氧化后的“海水”需要引入大量的显碱性的海水与之混合后才能排放,主要目的是中和、稀释经氧气氧化后海水中生成的酸(H+),
故答案为:2H2SO3+O2=2H2SO4;中和经氧气氧化后海水中生成的酸【或中和酸;降低氧化后溶液的酸性】;
(3)①溴易挥发,升高温度促进其挥发,所以通入热空气的目的是吹出Br2,
故答案为:将Br2吹出;
②因Br-和BrO3-在酸性条件下发生归中反应生成Br2:5NaBr+NaBrO3+3H2SO4═3Br2+3Na2SO4+3H2O,该反应中Br元素化合价由+5价、-1价变为0价,所以溴既是氧化产物也是还原产物,且有$\frac{1}{6}$的溴来自于BrO3-,若有1mol溴单质生成,转移电子物质的量=1mol×2×$\frac{1}{6}$×(5-0)=$\frac{5}{3}$mol≈1.67mol,
故答案为:1.67.
点评 本题考查较综合,涉及氯气储存、海水脱硫、海水中提溴、氧化还原反应计算等,综合考查学生分析能力、知识综合应用能力,题目难度中等.


 学业测评一课一测系列答案
学业测评一课一测系列答案 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案科目:高中化学 来源: 题型:选择题
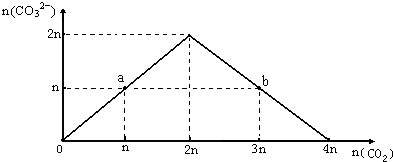 向NaOH溶液中缓慢通入CO2气体,溶液中CO32-的物质的量与通入CO2物质的量的关系图如下.下列关于图中a、b两点溶液的说法错误的是( )
向NaOH溶液中缓慢通入CO2气体,溶液中CO32-的物质的量与通入CO2物质的量的关系图如下.下列关于图中a、b两点溶液的说法错误的是( )| A. | a、b溶液与同浓度盐酸完全反应时,消耗盐酸的体积相同 | |
| B. | a溶液中水的电离程度与b溶液中水的电离程度相同 | |
| C. | a、b两溶液都满足:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-) | |
| D. | 将a、b两点混合后溶液满足:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径大小关系为Z>Y>X | |
| B. | 由X、Z、M、W四种元素形成的化合物都不能用于焙制糕点的食品工业 | |
| C. | 由X、Y、Z、M四种元素形成的所有化合物既能和强酸反应又能和强碱反应 | |
| D. | 由X与M形成的不同分子的空间构型可能是正四面体型、直线型或平面型等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 决定某化学反应反应速率的主要因素是催化剂 | |
| B. | 青霉素、橡胶、阿斯匹林全部由化学合成制得 | |
| C. | 铝有还原性,在反应中放出大量热能用来冶炼难熔金属Mn等 | |
| D. | 陶瓷品、酒精、乙烯塑料等的使用不会对环境造成污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 是a mL | B. | 是(50-a)mL | C. | 一定大于a mL | D. | 一定大于(50-a)mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液、蒸馏、萃取 | B. | 萃取、蒸发、分液 | C. | 分液、萃取、蒸馏 | D. | 蒸馏、萃取、分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5mol/LNaCl溶液 | B. | 1L3mol/LNa2SO4溶液 | ||
| C. | 0.4mol/LNaOH溶液 | D. | 2L0.15mol/LNa3PO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4LCO和CO2的混合气体中所含的碳原子数一定是NA | |
| B. | 含1molHCl的盐酸溶液与足量Fe反应,Fe所失去的电子总数为2NA | |
| C. | 常温常压下,32gO2和32gO3所含氧原子数都是2NA | |
| D. | 1mol/L的Na2SO4溶液中含2NA个Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用10mL量筒量取6.8mL稀H2SO4 | |
| B. | 用碱式滴定管量取15.80mLKMnO4溶液 | |
| C. | 酸碱中和滴定时,滴定管需用标准液或待测液润洗 | |
| D. | 中和热测定时,氢氧化钠溶液稍过量的目的是为了保证盐酸完全被中和 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com