
ij��ѧ��ȤС����ʵ����������������ͭ��ҺΪ���Һ���õ��ķ���ʵ���˴�ͭ(����������п������������Ƚ�����������������)���ᴿ������������͵��Һ�н������л��պͺ����ⶨ����ش��������⡣
��1�����ʱ����ͭӦ���Դ�� �������������ϵĵ缫��ӦʽΪ ���������У�����ͭ��Ũ�Ȼ� (ѡ�������䡱��С��)��
��2�������ɺ�С��ͬѧ�����Һ���˺����Һ��������ֱ���д�����
����������ۺ����ã�ϡ���ᴦ��������õ�������ϡ��Һ������д���ò���Ӧ�����ӷ���ʽ�� ��
��Cu�Ļ��ա���Һ�ɷּ������IJⶨ�������Ǹ�С����Ƶ�һ��ʵ�����̡�
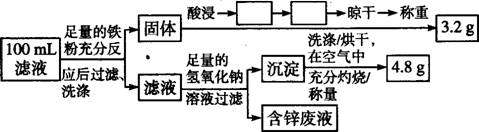
�����������пո���������Ӧ�IJ����� �� ��100 mL��Һ��Cu2+��Ũ��Ϊ mol/l��Fe2+��Ũ��Ϊ mol/l��
���𰸡���1���� Cu2++2e-��Cu ��С ��2�� �� 3Ag+4H++NO3-=3Ag++NO+2H2O �� ���� ϴ�� 0.5 0.1
��������
�����������1�����ʱ����ͭӦ���Դ����������������������������ͭ���ӵõ����ӣ��缫��ӦʽΪCu2++2e-��Cu������������ͭ�л��л��õĽ���ʧȥ���ӣ���������ʼ������Һ�е�ͭ���ӷŵ磬��˵������У�����ͭ��Ũ�Ȼ��С��
��2���ٽ��������Ժ�ϡ���ᷴӦ������������һ��������ˮ����3Ag+4H++NO3-��3Ag++NO��+2H2O��
��100mL����Һ�к����������ӡ�ͭ���ӡ�п���ӣ������������Ľ���Fe�ԺὫ����ͭȫ���û����������ù���������ͭ�Ļ�����������ܽ⣬Ҫ�õ�����ͭ����Ҫ���еIJ����ǹ��ˡ�ϴ�ӡ�����������������ɵ�3.2g������Cu�����ʵ�����3.2g��64g/mol��0.05mol������ͭ���ӵ�Ũ��c��0.05mol��0.1L��0.5 mol/L���������Ӻ��������Ʒ�Ӧ�����������������ڿ����и��ױ�����Ϊ�������������ȷֽ����ɵ���������������4.8g�����ʵ�����4.8g��160g/mol��0.03mol������ԭ���غ㣬�������ӵ����ʵ����ǣ�0.03mol��2��0.06mol��������ͭ���ӷ�Ӧ���������ʵ�����0.05mol�������������ӵ����ʵ�����0.05mol������ԭ��Һ���������ӵ����ʵ�����0.06mol��0.05mol��0.01mol��Ũ��c��0.01mol��0.1L��0.1mol/L��
���㣺�����⾫��ͭ�Լ����ʵĺ����ⶨ��ʵ�鷽�����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��������Һ�У���������һ���ܹ������������(����)
A��ʹ��̪��Һ������Һ��Na����Cl����SO42����Fe3��
B��ʹ��ɫʯ����Һ������Һ��Fe2����Mg2����MnO4����Cl��
C��pH<7����Һ��K����Ba2����Cl����Br��
D��̼��������Һ��K����SO42����Cl����H��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1����4�֣����õ���̬����������������������
�ٿ�����������ĸ���ָ����Է�ӳ�����صĿ������������и�����Ŀǰδ�����ҹ���������������� �� ��ѡ����ĸ����ͬ���� a��SO2 b��NO2 c��CO2 d��PM2.5 e���ȷ���
������Ӧ�����ռ�����������Ӧ���������С�  ����־����Ͳ���� �� ��
����־����Ͳ���� �� ��
a���ϵ�� b�������Ƶ������� c���������������
�۽��գ��������سɹ��ƻ���һ���ش����á��ع��͡�����ʳ���Ͱ������ۺ����á��ع��͡���һ�ַ�����ͨ�������ع��͡����мӹ��ᴿ��ˮ�����ɻ�ȡ �� �� �� �������ƣ���
��2����7�֣����彡����ʳƷ��ҩ��ȹ�ϵ���С�
�ٺ���������ʳ�����ǵĽ������������ʹ��䣺ţ�̡���������͡�ˮ���ȣ����к��е�Ӫ��������֬�����ࡢ �� �� �� �����κ�ˮ��
��������Ӧ��������ȡ��������Ԫ�أ����� �� Ԫ�غ���������ͣ��������״�ټ�������������ȱ��ʱ�����ܻ��еļ����� �� ��a��ƶѪ b���������� c��ҹä֢
�� ��������������������θ����࣬��д���÷�Ӧ�����ӷ���ʽ �� ��
����ù���ʺ����Ƶļ����� �� ��a����ð���� b��ϸ����Ⱦ c��θ�����
��3����4�֣�������������������ͷ�չ����Ҫ���ʻ�����
�������в����У������л��߷��Ӳ��ϵ��� �� �����ڸ��ϲ��ϵ��� �� ��
a��Ӳ�� b��������ϩ���� c���������մ� d��������
�ڹ�����ˮ���dz��õĽ������ϣ�����Ҫ���� �� �����Ϊԭ���Ƴɡ�
�۸����ڳ�ʪ�Ŀ�������Ҫ�����ĵ绯ѧ��ʴ�� �� ��ʴ��ͨ���öۻ���Ϳ�ᡢ��Ƶȷ�������ֹ��ʴ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��NA��ʾ�����ӵ�������ֵ������������ȷ����
A����״���£�22.4 L NO��11.2 L O2��ַ�Ӧ��õ������������ΪNA
B��3.6 g��ˮ�к��е�������Ϊ2NA
C��һ�������£�6.4 gͭ���������Ӧ��ת�Ƶ�����ĿΪ0.2NA
D�������£�1 L 1 mol��L��1��CH3COOH��Һ�У��������ʷ�����С��NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
Ϊ��̽����������Է�ӦaX��g��+bY��g�� cZ��g����Ӱ�죬��X��Y�����ʵ�����Ϊa��b��ʼ��Ӧ��ͨ��ʵ��õ���ͬ�����´ﵽƽ��ʱZ�����ʵ���������ʵ������ͼ��ʾ�������ж���ȷ����
cZ��g����Ӱ�죬��X��Y�����ʵ�����Ϊa��b��ʼ��Ӧ��ͨ��ʵ��õ���ͬ�����´ﵽƽ��ʱZ�����ʵ���������ʵ������ͼ��ʾ�������ж���ȷ����

A����H��0��a+b��c B����H��0��a+b��c
C����H��0��a+b��c D����H��0��a+b��c
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���н�����ʵ�Ļ�ѧ����ʽ�����ӷ���ʽ����ȷ���ǣ�������
| �� | A�� | ��Na2CO3�м������CO2���壺CO32﹣+CO2+H2O=2HCO3﹣ |
| �� | B�� | �ڷ�ˮ�е��뱥��FeCl3��Һ��ȡFe��OH��3���壺Fe3++3H2O=Fe��OH��3�����壩+3H+ |
| �� | C�� | 4mol/L��NaAlO2��Һ��7mol/L������������ϣ�4AlO2﹣+7H++H2O=3Al��OH��3��+Al3+ |
| �� | D�� | �ữ��KMnO4��Һ��H2O2��Ӧ��2MnO4﹣+6H++5H2O2=2Mn2++5O2��+8H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
NA��ʾ�����ӵ�������ֵ������˵����ȷ���ǣ�������
| �� | A�� | 1molCl2�μӵ��κη�Ӧת�Ƶ���������2NA |
| �� | B�� | 1mol/L��NaCl��Һ�к���NA��Na+ |
| �� | C�� | ��״���£�22.4mlˮ�к��еķ�����ԼΪ1.24NA |
| �� | D�� | 1molFeCl3��ȫˮ������NA���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Zn��s��+H2SO4��l��=ZnSO4��l��+H2��g������H��0��kJ•mol��1���Ļ�ѧ��Ӧ����������һ����ȷ���ǣ�������
| �� | A�� |
��Ӧ������������ϵ������ͼ��ʾ |
| �� | B�� | 1mol���������1molH2���������� |
| �� | C�� | �����÷�Ӧ��Ƴ�ԭ��أ���пΪ���� |
| �� | D�� | ���������Ϊԭ��أ�����32.5gп�ܽ�ʱ�������ų����������һ��Ϊ22.4L������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����£��ú� 0.2mol NaOH����Һǡ������0.2mol NO2���1L��Һ����Ӧ�Ļ�ѧ����ʽΪ��2NO2+2NaOH��NaNO3+NaNO2+H2O���Է�Ӧ�����Һ������˵����ȷ���ǣ���֪��Ka��HNO2��=7.1��10��4��Ka��CH3COOH��=1.7��10��5����������
| �� | A�� | n��NO2����+n��OH������n��H+��=0.1 mol |
| �� | B�� | ��ͨ��0.01 mol HCl���壬��ҺpH����2��������Һ����ı仯�� |
| �� | C�� | ����������CH3COONa���壬��Һ�ļ��Ի���� |
| �� | D�� | ��ʱ��Һ��pH����0.1 mol/L��CH3COONa��Һ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com