
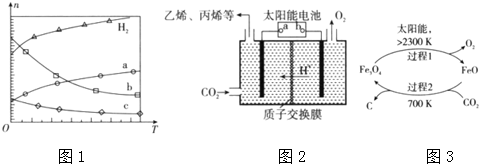
���� ��1�������߱仯��֪�����¶����ߣ����������ʵ��������࣬˵�������¶�ƽ�������ƶ���������Ӧ���ȣ���֪aΪCO2�ı仯���ߣ���ϼ�������ϵ��֪bΪˮ��cΪC2H4�ı仯���ߣ�
��2��̫���ܵ��Ϊ��Դ�����ǿ���ԵĶ�����̼ˮ��Һ�õ���ϩ����ϩ���������ɣ��ݴ˽��
��3���ٷ�Ӧ2Fe3O4$\frac{\underline{\;2300K\;}}{\;}$6FeO+O2����OԪ�ػ��ϼ���-2�����ߵ�0�ۣ����Ԫ�ػ��ϼ��Լ�����ʽ���㣻
����ʾ��ͼ��֪������2��CO2��FeO��Ӧ����Fe3O4��C���ݴ˽�ɣ�
��� �⣺��1���������߱仯��֪�����¶����ߣ����������ʵ��������࣬˵�������¶�ƽ�������ƶ���������Ӧ���ȣ��ʴ�Ϊ������
�������¶����ߣ����������ʵ��������࣬������Ϊ��Ӧ�����һ�������������ΪCO2���ɼ�������ϵ��֪bΪˮ��cΪC2H4�ı仯���ߣ��ʴ�Ϊ��H2O��
��Ϊ���CO2��ƽ��ת���ʣ����ı��¶��⣬���ɲ�ȡ�Ĵ�ʩ������ѹǿ���ʴ�Ϊ����ѹ��
��2����̫���ܵ��Ϊ��Դ�����ǿ���ԵĶ�����̼ˮ��Һ�õ���ϩ����֪����ת����ʽ�й���ת��Ϊ���ܣ�����ת��Ϊ��ѧ�ܣ����ֵ���ת��Ϊ���ܣ��ʴ�Ϊ��̫����ת��Ϊ���ܣ�����ת��Ϊ��ѧ�ܣ�
�ڵ��ʱ��������̼��b����������ϩ���õ����ӵ�һ��Ϊ��Դ���������缫��ӦʽΪ2CO2+12H++12e-=C2H4+4H2O���ʴ�Ϊ������2CO2+12H++12e-=C2H4+4H2O��
��3���ٷ�Ӧ2Fe3O4$\frac{\underline{\;2300K\;}}{\;}$6FeO+O2����OԪ�ػ��ϼ���-2�����ߵ�0�ۣ��ɷ���ʽ��֪��2molFe3O4�μӷ�Ӧ������1mol������ת��4mol���ӣ���ÿ�ֽ�lmolFe3O4ת�Ƶ��ӵ����ʵ���Ϊ2mol���ʴ�Ϊ��2mol��
����ʾ��ͼ��֪������2��CO2��FeO��Ӧ����Fe3O4��C����Ӧ�ķ���ʽΪ6FeO+CO2$\frac{\underline{\;700K\;}}{\;}$2Fe3O4+C���ʴ�Ϊ��6FeO+CO2$\frac{\underline{\;700K\;}}{\;}$2Fe3O4+C��
���� �����漰������ԭ����ѧƽ���ƶ��Լ�ԭ��ط�Ӧ��֪ʶ��������ѧ���������⡢����������������Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Na2SiO3��Һ��ͨ�����CO2��SiO32-+CO2+H2O�TH2SiO3+CO32- | |
| B�� | �����ữ�ĵ���KI��Һ�ڿ����б����ɫ��4I++O2+2H2O�T2I2+4OH- | |
| C�� | ��������������ʴʱ�������ĵ缫��Ӧʽ��O2+4e-+2H2O�T4OH- | |
| D�� | ���������������������Ҫ��Ӧ��4NH3+7O2$\frac{\underline{\;����\;}}{����}$4NO2+6H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SO2����ͨ��NaOH��Һ�У�������������˵��SO2��������ˮ | |
| B�� | SO2����ͨ����ˮ�У���ˮ����ɫ��ȥ��˵��SO2����Ư���� | |
| C�� | SO2����ͨ������KMnO4��Һ�У���Һ����ɫ��dz��˵��SO2���л�ԭ�� | |
| D�� | SO2����ͨ��Ba��NO3��2��Һ�У���Һ���ֻ�������˵����BaSO3�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
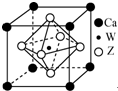 ԭ������С��36��X��Y��Z��W����Ԫ�أ�X��̬ԭ�ӵ����������������ڲ��������2����Y��̬ԭ�ӵ�2pԭ�ӹ������3��δ�ɶԵ��ӣ�Z�ǵؿ��к�������Ԫ�أ�W��ԭ������Ϊ22��
ԭ������С��36��X��Y��Z��W����Ԫ�أ�X��̬ԭ�ӵ����������������ڲ��������2����Y��̬ԭ�ӵ�2pԭ�ӹ������3��δ�ɶԵ��ӣ�Z�ǵؿ��к�������Ԫ�أ�W��ԭ������Ϊ22���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 mol FeI2������������Ӧʱת�Ƶĵ�����Ϊ2NA | |
| B�� | 1 L 1mol/L�����Ậ��NA��HCl���� | |
| C�� | ��״���£�33.6 L���Ȼ�̼�к�����ԭ�ӵ���ĿΪ6NA | |
| D�� | 5NH4NO3$\frac{\underline{\;\;��\;\;}}{\;}$2HNO3+4N2��+9H2O��Ӧ�У�����28 g N2ʱ��ת�Ƶĵ�����ĿΪ3.75NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | DԪ�ش���Ԫ�����ڱ��е�3���ڵڢ��� | |
| B�� | ����Ԫ�ص�ԭ�Ӱ뾶��r��A����r��B����r��C����r��D�� | |
| C�� | B��D������������У�B��D����ԭ�Ӿ�Ϊ˫�� | |
| D�� | һ�������£�B������ת����D���ʣ�C���������û���A���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �÷�Ӧ���ӳɷ�Ӧ | B�� | ��ϩ����ͨ��ʯ���ѽ��� | ||
| C�� | �Ҵ�������Ϊ�ǻ� | D�� | �Ҵ�����ȩ�����ụΪͬϵ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| �¶� | ʱ��/min n/mol | 0 | 10 | 20 | 40 | 50 |
| T1 | n�� N2�� | 0 | 0.20 | 0.35 | 0.40 | 0.40 |
| T2 | n�� N2�� | 0 | 0.25 | �� | 0.30 | 0.30 |
| A�� | 10min�ڣ�T1ʱ��v��N2����T2ʱ��С | |
| B�� | T1��T2 | |
| C�� | a��0 | |
| D�� | T2ʱ������ƽ�����������ٳ���1.2molCH4�����´ﵽƽ��ʱn��N2��=0.40mol |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com