
| 元素代号 | K | L | M | Q | R | T | N |
| 原子半径/nm | 0.183 | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 | 0.152 |
| 主要化合价 | +1 | +2 | +3 | +6、-2 | +2 | -2 | +1 |
| A. | K、L、M三种元素的金属性逐渐减弱 | |
| B. | 在RCl2分子中,各原子均满足8电子的稳定结构 | |
| C. | Q元素的最高价氧化物为非电解质,其水溶液能够导电 | |
| D. | K在T单质中燃烧所形成的化合物中含有非极性共价键和离子键 |
分析 短周期元素,由元素的化合价可知,T只有-2价,则T为O元素,可知Q为S元素,K、L、R只有正价,L、R都是+2价,原子半径L>R,则L为Mg元素,R为Be元素,K显+1价,原子半径大于L,则K为Na元素,原子半径K>L>M,则M为Al元素,N显+1价,原子半径N>R,则N为Li元素,结合元素周期律和原子结构及物质的性质、化学键的相关知识答题.
解答 解:短周期元素,由元素的化合价可知,T只有-2价,则T为O元素,可知Q为S元素,K、L、R只有正价,L、R都是+2价,原子半径L>R,则L为Mg元素,R为Be元素,K显+1价,原子半径大于L,则K为Na元素,原子半径K>L>M,则M为Al元素,N显+1价,原子半径N>R,则N为Li元素,
A、K为Na元素,L为Mg元素,M为Al元素,Na、Mg、Al元素的金属性逐渐减弱,故A正确;
B、R为Be元素,BeCl2分子中,Be原子最外层只有4个电子,故B错误;
C、Q为S元素,SO3为非电解质,SO3溶于水生成硫酸,溶液能导电,故C正确;
D、K为Na元素,T为O元素,钠在氧气中燃烧,生成过氧化钠中既有离子键又有非极性共价键,故D正确.
故选B.
点评 本题考查元素的性质与位置关系,学生能利用原子半径及化合价来推断出元素是解答本题的关键,并熟悉元素及其单质、化合物的性质及元素周期律等来解答即可,难度不大.


 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案科目:高中化学 来源: 题型:选择题
| X | Y | ||
| Z | W | Q |
| A. | X、W分别与钠形成的化合物摩尔质量相同,且每种化合物中阴阳离子数比为1:2 | |
| B. | 含X和Z元素的常见化合物为离子化合物 | |
| C. | 氧化物对应的水化物酸性:W<Q | |
| D. | 原子半径大小关系:Q>W>Z>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
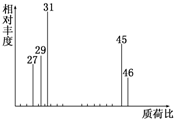 为了测定某有机物A的结构,做如下实验:
为了测定某有机物A的结构,做如下实验:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向FeI2的溶液中,通入足量Cl2:2Fe2++2I-+2Cl2═I2+2Fe3++4Cl- | |
| B. | Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+═Fe3++3H2O | |
| C. | 向水玻璃中通入过量的CO2:SiO32-+2CO2+2H2O═H2SiO3↓+2HCO3- | |
| D. | 酸性条件下KIO3溶液与KI溶液发生反应生成I2:IO3-+5I-+3H2O═3I2+6OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 117 g该元素原子的物质的量为1 mol | |
| B. | 该元素一定为非金属元素 | |
| C. | 该元素在地球上的含量十分丰富 | |
| D. | 该元素的金属性可能比非金属性更明显 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
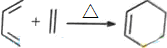 .根据下列转化流程,回答问题:
.根据下列转化流程,回答问题: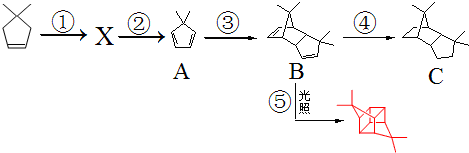
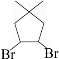 .
.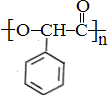 的合成路线:
的合成路线: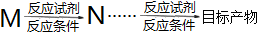 )
)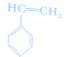 $\stackrel{Br_{2}}{→}$
$\stackrel{Br_{2}}{→}$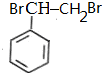 $→_{△}^{NaOH溶液}$
$→_{△}^{NaOH溶液}$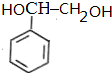 $\stackrel{[O]}{→}$
$\stackrel{[O]}{→}$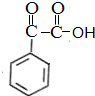 $→_{催化剂}^{H_{2}}$
$→_{催化剂}^{H_{2}}$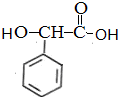 $\stackrel{浓H_{2}SO_{4}△}{→}$
$\stackrel{浓H_{2}SO_{4}△}{→}$ .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
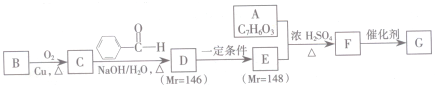

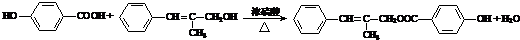 .
. .
. (其中任一种).
(其中任一种).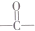 结构②苯环上有2个取代基.
结构②苯环上有2个取代基.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com