
| 12 |
| 12��0.5 |


 ��������ϵ�д�
��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���������ᷴӦ��2Fe+6H+=2Fe3++3H2�� |
| B���Ȼ�����ͭ��Ӧ��Fe3++Cu=Fe2++Cu2+ |
| C������ʯ��ˮ��̼������Һ��ϣ�Ca��OH��2+CO32-=CaCO3��+2OH- |
| D���ô����ˮ����2CH3COOH+CaCO3=2CH3COO-+Ca2++H2O+CO2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
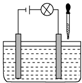 ����ͼ��ʾ�������Һ�ĵ�����װ���У�����ijһ�������Һ����μ�����һ����Һʱ����ƹ������䰵��Ϩ������������ǣ�������
����ͼ��ʾ�������Һ�ĵ�����װ���У�����ijһ�������Һ����μ�����һ����Һʱ����ƹ������䰵��Ϩ������������ǣ�������| A����������μ���ʳ����Һ |
| B����������μ�������������Һ |
| C������ʯ��ˮ�в���ͨ��CO2 |
| D����������μ��백ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��10�� | B��9�� | C��8�� | D��7�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������C��H��Oԭ�Ӹ�����Ϊ14��12��3 |
| B������̼���⡢������Ԫ����� |
| C���������У�̼���⡢������Ԫ�ص�������Ϊ14��12��3 |
| D������Ħ������Ϊ228g?mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� | CH4 | CO2 | CO | H2 |
| ������� | 0.1 | 0.1 | 0.4 | 0.4 |

| ʵ���� | �������/L | �¶�/�� |
| �� | 1.0 | 1200 |
| �� | 2.0 | 1200 |
| �� | 2.0 | 1300 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ������/��kJ?mol-1�� | I1 | I2 | I3 | I4 |
| A | 932 | 1 821 | 15 390 | 21 771 |
| B | 738 | 1 451 | 7 733 | 10 540 |
 ��ÿ��COCl2�����ں���
��ÿ��COCl2�����ں����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com