
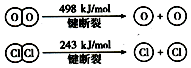
 已知4HCl(g)+O2(g) $?_{400℃}^{催化剂}$2Cl2(g)+2H2O(g)中2mol HCl被氧化,放出57.8kJ的热量,且部分化学键断裂示意图如下:
已知4HCl(g)+O2(g) $?_{400℃}^{催化剂}$2Cl2(g)+2H2O(g)中2mol HCl被氧化,放出57.8kJ的热量,且部分化学键断裂示意图如下:分析 ①反应4HCl(g)+O2(g) $?_{400℃}^{催化剂}$2Cl2(g)+2H2O(g)中2mol HCl被氧化,放出57.8kJ的热量,据此可计算出4molHCl被氧化放出热量;
②焓变=反应物断键吸收热量-生成物形成化学键放出热量,据此列式计算出断开1mol H-O键与断开 1mol H-Cl 键所需能量之差;根据计算结果判断二者键能大小.
解答 解:①反应4HCl(g)+O2(g) $?_{400℃}^{催化剂}$2Cl2(g)+2H2O(g)中2mol HCl被氧化,放出57.8kJ的热量,则4molHCl被氧化放出115.6kJ热量,该反应的热化学方程式为:4HCl(g)+O2(g)?2Cl2(g)+2H2O(g)△H=-115.6 kJ/mol,
故答案为:-115.6;
②焓变=反应物断键吸收热量-生成物形成化学键放出热量,4HCl(g)+O2(g)?2Cl2(g)+2H2O(g)△H=-115.6 KJ/mol,
则:4×E(H-Cl)+498-[243×2+4×E(H-O)]=-115.6,即:4×E(H-O)-4×E(H-Cl)=498-486+115.6=127.6,
所以E(H-O)-E(H-Cl)=31.9≈32,H2O中H-O键比HCl中H-Cl键强,
故答案为:32;强.
点评 本题考查了反应热与焓变的应用,题目难度不大,明确反应热与键能的关系为解答关键,注意掌握化学反应与能量变化的关系,试题培养了学生的分析能力及灵活应用能力.


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:选择题
| A. | Na+、HCO3-、SO42-、Cl- | B. | Cu2+、NO3-、Cl-、SO42- | ||
| C. | H+、Cl-、K+、CO32- | D. | K+、Mg2+、SO42-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
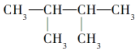 的系统命名为2,3-二甲基丁烷;
的系统命名为2,3-二甲基丁烷;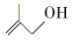 的分子式为C4H8O;
的分子式为C4H8O;查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 两烧杯中铜片表面均无气泡产生 | B. | 甲中化学能转化成了电能 | ||
| C. | 甲中铜片是负极 | D. | 乙中铜片是正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
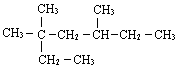 3,3,5-三甲基庚烷
3,3,5-三甲基庚烷 2,3-二甲基1-丁烯
2,3-二甲基1-丁烯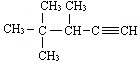 的系统名称为3,4,4-三甲基-1-戊炔
的系统名称为3,4,4-三甲基-1-戊炔 表示的分子式C6H14;名称是2-甲基戊烷.
表示的分子式C6H14;名称是2-甲基戊烷.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色溶液中:Al3+、NH4+、Cl-、HCO3- | |
| B. | 甲基橙显红色的溶液中:Fe2+、Na+、SO42-、NO3- | |
| C. | 水电离出来的c(H+)=10-12mol•L-1的溶液:K+、HCO3-、I-、ClO- | |
| D. | pH值为1的溶液:Fe2+、Cl-、Na+、SCN- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将lmol Cl2溶于水,所得溶液中HClO、Cl-和C1O-的总数目为2NA | |
| B. | 46g NO2和N2O4混合物中含分子数为NA | |
| C. | 氢氧燃料电池正极消耗22.4L气体时,电路中通过的电子数目为4NA | |
| D. | 适量Na2O2与CO2反应生成1mol O2时,转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所含质子数=A-n | B. | 所含中子数=A-Z | C. | 所含电子数=Z+n | D. | 质量数=A+Z |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com