
某可逆反应正向反应过程中能量变化如图所示,下列说法不正确的是 ( )
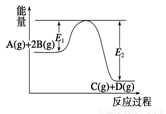
A.压强增大,平衡向正反应方向移动
B.当反应达到平衡时,降低温度,A的转化率增大
C.升高温度,平衡常数K减小;
D.加入催化剂,反应速率增大,E1减小,E2减小,反应热减小
科目:高中化学 来源:2015-2016学年浙江省宁波市高一下学期学考期中化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值,下列说法正确的是
A.若5.6 LN2中含有n个氮分子,则阿伏加德罗常数一定为4n
B.4.6 g Na与100 mL含0.1 mol HC1的盐酸溶液反应,转移电子数目为0.2NA
C.14 g乙烯和丙烯的混合气体中所含分子总数为0.5NA
D.标准状况下,22.4 L CCl4含有的分子总数为NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省宁波市高二下学期期中考试化学试卷(解析版) 题型:选择题
能大量共存于同一溶液中,且当加入另一种强电解质使水电离出的c(H+) = 1×10-13 mol/L时又一定能发生反应的离子组是
①Na+ 、Ba2+ 、Cl- 、HCO3- ②K+ 、NH4+ 、CH3COO- 、SO42-
③Ca2+ 、Cu2+ 、 NO3- 、SO32- ④Fe3+ 、Na+ 、SCN- 、Cl-
⑤Al3+ 、Na+ 、HCO3- 、NO3- ⑥Fe2+ 、Na+ 、NO3-、I-
⑦Ag+ 、NH4+ 、OH- 、NO3- ⑧Na+ 、K+ 、CH3COO- 、NO3-
A.①②⑥ B.②③⑥ C. ①② D. ③⑤⑦
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省宁波市高二下学期期中考试化学试卷(解析版) 题型:选择题
物质的鉴别有多种方法。下列能达到鉴别目的的是
① 用水鉴别苯、乙醇、溴苯 ② 用相互滴加的方法鉴别Ca(OH)2和NaHCO3溶液③ 点燃鉴别甲烷和乙炔
A.① ② B.①③ C.②③ D.①②③
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一下学期期中考试化学试卷(解析版) 题型:填空题
煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程。
(1) 将水蒸气通过红热的碳即可产生水煤气。反应为:
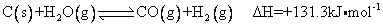
一定温度下,在一个容积固定的密闭容器中,发生上述反应,下列不能判断该反应达到化学平衡状态的是_______ (填字母)。
a.容器中的压强不变
b.1 mol H-H键断裂的同时断裂2 mol H-O键
c.υ正(CO)=υ逆(H2)
d.c (CO) = c (H2) e、υ(H2O):υ(CO):υ(H2)=1:1:1
(2) 将不同量的CO(g)和H2O(g)分别通入到体积为2 L的恒容密闭容器中,进行反应
CO(g)+H2O(g) ? CO2 (g)+H2 (g) ,得到如下三组数据:
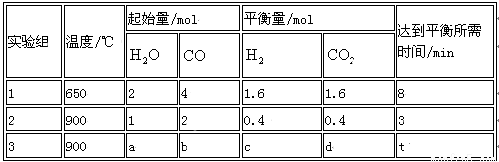
① 实验1中从开始到达平衡时CO表示反应的平均速率为 mol/(l·min),CO(g)的转化率为 。
② 实验2中H2O(g)的转化率为 ,该反应的逆反应为_______ (填“吸”或“放”)热反应。
③ 若实验3平衡时要达到与实验2中平衡时各物质的质量分数分别相等,且t<3min,则a、b应满足的关系 是______________ (用含a、b的数学式表示)。
(3)目前工业上有一种方法是用CO2来生产甲醇。一定条件下发生反应:CO2 (g)+3H2 (g) ? CH3OH(g)+H2O(g)图(1)表示该反应进行过程中能量(单位为kJ?mol-1。)的变化。
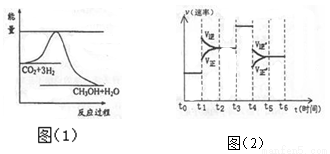
① 在体积为1 L的恒容密闭容器中,充入l molCO2和3molH2,下列措施中能使 c (CH3OH)增大的是_______ (填字母)
a.升高温度
b.充入He (g),使体系压强增大
c.将H2O(g)从体系中分离出来
d.再充入l mol CO2和3 molH2
② 当反应达到平衡时不断改变一个条件(但不改变各组分物质的量和状态)反应速率随时间的变化如图(2): 其中表示平衡混合物中CH3OH含量最高的一段时间是_______ ;t1~t2改变的条件为 若t0~t1平衡常数为K1, t2~t3平衡常数为K2 ,则K1 _______K2 (填“>”、“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一下学期期中考试化学试卷(解析版) 题型:选择题
为探究锌与盐酸反应过程的速率变化,某同学的实验测定方法是:在100ml稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(氢气体积已换算为标准状况):

下列说法正确的是:( )
A.0~1 min反应速率最大,因为此时反应物浓度最高
B.2~3min反应速率最大,因为此时反应物浓度相对较高,且反应放热使温度升高
C.3~4 min时间内以盐酸的浓度变化来表示的平均反应速率为0.5mol·L-1 ·min-1
D.4~5min反应速率最大,因为此时反应混合物的温度最高
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一下学期期中考试化学试卷(解析版) 题型:选择题
已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
A. 原子半径A>B>D>C B. 原子序数d>c>b>a
C. 离子半径C>D>B>A D. 单质的还原性A>B>D>C
查看答案和解析>>
科目:高中化学 来源:2016届云南省高三下第七次月考理综化学试卷(解析版) 题型:推断题
某有机物A(C4H6O5)广泛存在于许多水果内,尤以苹果、葡萄、西瓜、山楂内为多,是一种常用的食品添加剂。该化合物具有如下性质:
①在25℃时,A的电离平衡常数K1=3.9×10-4,K2=5.5×10-6
②A + RCOOH(或ROH) 有香味的产物
有香味的产物
③1 mol A 慢慢产生1.5 mol气体
慢慢产生1.5 mol气体
④核磁共振氢谱表明A分子中有5种不同化学环境的氢原子,与A相关的反应框图如下:
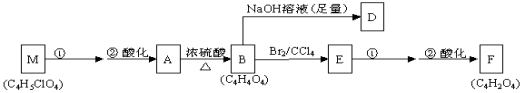
(1)根据化合物A的性质,对A的结构可作出的判断是_______。
(a)肯定有碳碳双键 (b)有两个羧基
(c)肯定有羟基 (d)有-COOR官能团
(2)写出A、D、F、M的结构简式:A:_________________;D:__________________;
F:_________________;M:__________________。
(3)写出A→B、B→E的反应类型:A→B______________; B→E_______________。
(4)写出M→A的第①步反应的反应条件:_______________________;
写出E→F的第①步反应的反应方程式: ___________________________________。
(5)在催化剂作用下,B与乙二醇可发生缩聚反应,生成的高分子化合物用于制造玻璃钢。写出该反应的化学方程式:__________________________________________。
(6)写出一种与A具有相同官能团的A的同分异构体的结构简式________________。
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三考前热身(五模)化学试卷(解析版) 题型:选择题
下列物质的转化在给定条件下不能实现的是
A.Ca(ClO)2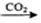 (aq)HClO(aq)
(aq)HClO(aq) HCl(aq)
HCl(aq)
B.H2SiO3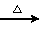 SiO2
SiO2 SiCl4
SiCl4
C.Al2O3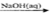 NaAlO2
NaAlO2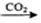 Al(OH)3
Al(OH)3
D.Fe2O3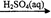 Fe2(SO4)3(aq)
Fe2(SO4)3(aq) 无水Fe2(SO4)3
无水Fe2(SO4)3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com