
分析 (1)金属钠与氢气反应生成白色的固体NaH;
(2)根据元素化合价能降低具有氧化性,化合价能升高具有还原性,既能升高又能降低则既具有氧化性又具有还原性;
(3)氢化钠与水反应生成氢氧化钠和氢气,方程式为NaH+H2O=NaOH+H2↑,H2O中H元素的化合价由+1价降低为0,NaH中H元素的化合价由-1价升高为0,化合价升高被氧化,化合价降低被还原,以此来解答.
解答 解:(1)金属钠与氢气反应生成白色的固体NaH,方程式为:2Na+H2$\frac{\underline{\;\;△\;\;}}{\;}$2NaH;故答案为:2Na+H2$\frac{\underline{\;\;△\;\;}}{\;}$2NaH;
(2)因为NaH中氢元素呈-1价,是氢的最低价,所以只有还原性,故答案为:还原性,因为NaH中氢元素呈-1价,是氢的最低价,只有还原性;
(3)氢化钠与水反应生成氢氧化钠和氢气,方程式为NaH+H2O=NaOH+H2↑,H2O中H元素的化合价由+1价降低为0被还原,NaH中H元素的化合价由-1价升高为0被氧化,由反应方程式可知,被氧化与被还原的H元素的原子个数比为1:1,则被氧化与被还原元素的质量比为1:1,
故答案为:1:1.
点评 本题考查方程式的书写以及氧化还原反应,明确氧化还原反应中元素的化合价变化及基本概念即可解答,题目难度不大.


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源:2017届江西省高三上第二次月考化学试卷(解析版) 题型:选择题
向下图装置中缓慢地通入气体X,若关闭活塞K,则品红溶液无变化,而澄清石灰水变浑浊;若打开活塞K,则品红溶液退色,加热后又恢复红色.据此判断气体X和洗气瓶内溶液Y分别可能是
A | B | C | D | NO2 | HCl | SO2[来 | |
Y | Na2SO3溶液 | 水 | Na2SO3溶液 | 饱和NaHCO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
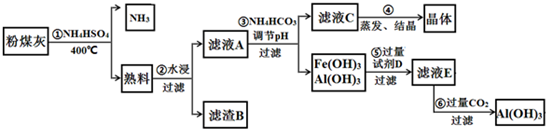
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,等体积的CH4和CO2分子数相等 | |
| B. | 与NaOH溶液、稀硫酸反应产生等量的H2,所需铝粉的质量相等 | |
| C. | 常温下,铜与浓硫酸迅速反应产生SO2气体 | |
| D. | 1mol OH-和17g NH3所含的电子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(NH3)=$\frac{2}{3}$v(H2O) | B. | v(O2)=$\frac{6}{5}$v(H2O) | C. | v(NH3)=$\frac{5}{4}$v(O2) | D. | v(O2)=$\frac{4}{5}$v(NO) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com