
【题目】利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实。某化学兴趣小组通过在实验室中模拟上述过程,其设计的模拟装置如下:
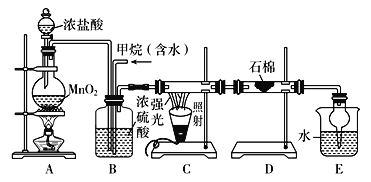
根据设计要求回答:
(1)B装置有三种功能:①控制气流速度; ②均匀混合气体; ③____________。
(2)设![]() =x,若理论上欲获得最多的氯化氢,则x取值范围________。
=x,若理论上欲获得最多的氯化氢,则x取值范围________。
(3)D装置的石棉中均匀混有KI粉末,其作用是______________。
(4)E装置的作用是________(填编号)。
A 收集气体 B 吸收氯气
C 防止倒吸 D 吸收氯化氢
(5)在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,写出置换出黑色小颗粒的化学方程式:_______________________________________。
(6)E装置中除生成盐酸外,还含有有机物,从E中分离出有机物的最佳方法为________。该装置还有缺陷,原因是没有进行尾气处理,其尾气主要成分为________(填编号)。
a CH4 b CH3Cl c CH2Cl2 d CHCl3 e CCl4
【答案】(1)干燥混合气体 (2)大于或等于4
(3)吸收过量的氯气 (4)CD
(5)CH4+2Cl2![]() C+4HCl
C+4HCl
(6)分液 ab
【解析】
(1)B装置的三个作用:①控制气流速度从而达到合适的反应比例;②均匀混合气体,便于后续实验;③干燥混合气体。
(2)当发生反应:CH4+4Cl2―→CCl4+4HCl时生成HCl气体最多,所以要保证![]() =x≥4。
=x≥4。
(3)KI能吸收多余的Cl2,反应的化学方程式为Cl2+2KI===2KCl+I2。
(4)E装置既吸收反应生成的HCl气体,同时还防止倒吸。
(5)据信息知黑色小颗粒应为碳粉,根据原子守恒可知反应方程式应为CH4+2Cl2![]() C+4HCl。
C+4HCl。
(6)分离难溶于水的油状液体可用分液法。


科目:高中化学 来源: 题型:
【题目】某学生用托盘天平称量食盐时,他将食盐放在右盘,砝码放在左盘,称得食盐的质量为15.5 g(1g以下使用游码)。该学生所称量的食盐的实际质量是( )
A.15.5 gB.15.0 gC.16.0 gD.14.5g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,对于密闭容器中进行的可逆反应A(g)+3B(g) ![]() 2C(g),下列说 法中,能说明这一反应已经达到化学平衡状态的是
2C(g),下列说 法中,能说明这一反应已经达到化学平衡状态的是
A. 生成C的速率是生成A的速率的两倍
B. A、B、C的浓度相等
C. 单位时间生成 n mol A,同时生成 3n mol B
D. A、B、C的分子数之比为 1∶3∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列各题。
(1)化合物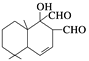 是一种取代有机氯农药DDT的新型杀虫剂,它含有的官能团有______________(写名称),它属于________(填“脂环”或“芳香”)化合物。
是一种取代有机氯农药DDT的新型杀虫剂,它含有的官能团有______________(写名称),它属于________(填“脂环”或“芳香”)化合物。
(2)酚酞是常用的酸碱指示剂,其结构简式如下所示:
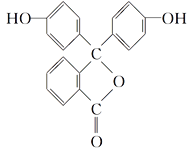
①酚酞的化学式为____________。
②从结构上看酚酞可看作____________(填字母)。
A.烯烃 B.芳香化合物 C.醇 D.酚 E.醚 F.酯
(3)莽草酸是从中药八角茴香中提取的一种有机物,具有抗炎、镇痛作用,常用作抗病毒和抗癌药物的中间体。莽草酸的结构简式为

请回答下列问题:
①在横线上写出官能团的名称________。
②莽草酸的分子式为________________。
③从对有机化合物按官能团分类的角度考虑,莽草酸属于________类、________类。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下将NaOH溶液添加到己二酸(H2X)溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述错误的是
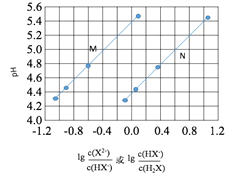
A. Ka2(H2X)的数量级为10-6
B. 曲线N表示pH与 的变化关系
的变化关系
C. NaHX溶液中c(H+)>c(OH-)
D. 当混合溶液呈中性时,c(Na+)>c(HX-)>c(X2-)>c(H+)=c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的电解池Ⅰ和Ⅱ中,a、b、c和d均为Pt电极。电解过程中,电极b和d上
没有气体逸出,但质量均增大,且增重b>d。符合上述实验结果的盐溶液是

选项 | X | Y |
A | MgSO4 | CuSO4 |
B | AgNO3 | Pb(NO3)2 |
C | FeSO4 | Al2 (SO4)3 |
D | CuSO4 | AgNO3 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在AlCl3和MgCl2的混合液中滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如下图所示,则原溶液中AlCl3和MgCl2的物质的量之比为( )
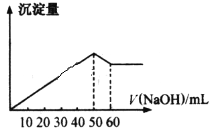
A. 1:2B. 1:1C. 2:1D. 3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究化学反应中的能量变化有重要意义。请根据学过的知识回答下列问题:
(1)已知一氧化碳与水蒸气反应过程的能量变化如图所示:
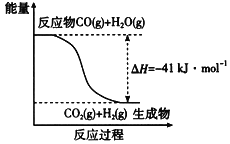
反应的热化学方程式为____________________________。
(2)化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知:N≡N键的键能是948.9 kJmol1,H—H键的键能是436.0 kJmol1,N—H键的键能是391.55 kJmol1,则![]() N2(g)+
N2(g)+![]() H2(g)
H2(g)![]() NH3(g) ΔH=_____________________。
NH3(g) ΔH=_____________________。
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:①C(s,石墨)+O2(g) ![]() CO2(g) ΔH1=393.5 kJmol1;②2H2(g)+O2(g)
CO2(g) ΔH1=393.5 kJmol1;②2H2(g)+O2(g) ![]() 2H2O(l) ΔH2=571.6 kJmol1;③2C2H2(g)+5O2(g)
2H2O(l) ΔH2=571.6 kJmol1;③2C2H2(g)+5O2(g) ![]() 4CO2(g)+2H2O(l)ΔH3=2599 kJmol1。298 K时反应2C(s,石墨)+H2(g)C2H2(g)的焓变:ΔH=_____________________。
4CO2(g)+2H2O(l)ΔH3=2599 kJmol1。298 K时反应2C(s,石墨)+H2(g)C2H2(g)的焓变:ΔH=_____________________。
(4)已知:铝热反应是放热反应,又知,常温下: 4Al(s)+3O2(g) ![]() 2Al2O3(s) ΔH1;4Fe(s)+3O2(g)
2Al2O3(s) ΔH1;4Fe(s)+3O2(g) ![]() 2Fe2O3(s) ΔH2。下面关于ΔH1、ΔH2的比较正确的是________。
2Fe2O3(s) ΔH2。下面关于ΔH1、ΔH2的比较正确的是________。
A.ΔH1>ΔH2 B.ΔH1<ΔH2 C.ΔH1=ΔH2 D.无法计算
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com