
| A、氧化剂 | B、还原剂 |
| C、催化剂 | D、漂白剂 |
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案科目:高中化学 来源: 题型:
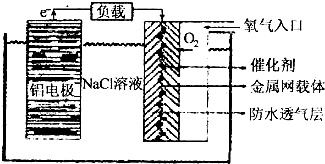
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、容量中残留少量蒸馏水 |
| B、定容时俯视观察液面 |
| C、定容时仰视观察液面 |
| D、没有把洗涤烧杯和玻棒的溶液注入容量瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe3+、NH4+、SCN-、Cl- |
| B、Na+、H+、NO3-、SO42- |
| C、Al3+、Fe2+、NO3-、Cl- |
| D、K+、Na+、Cl-、SiO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1L 0.2mol?L-1CH3COONa溶液中含有0.2NA个CH3COO- |
| B、标准状况下,11.2LCl2溶于水,转移的电子数为NA |
| C、常温常压下,23g NO2和N2O4的混合气体含有的原子数为1.5NA |
| D、100mL 18.4mol?L-1浓硫酸与足量铜加热反应,生成SO2的分子数为0.92NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、I2(g)+H2(g)?2HI(g),单位时间内消耗H2和HI的物质的量之比大于1:2 |
| B、N2(g)+3H2(g)?2NH3(g),改变某一条件后NH3的体积分数增大 |
| C、N2O4?2NO2(g),改变条件后气体颜色加深 |
| D、2SO2(g)+O2(g)?2SO3(g),改变条件后混合气体的平均相对分子质量减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com