
£Ø8·Ö£©ČēĶ¼ĖłŹ¾£¬¼×”¢ŅŅ”¢±ūŹĒČżÖÖ³£¼ūµ„ÖŹ£¬X”¢Y”¢ZŹĒ³£¼ū»ÆŗĻĪļ£¬ĖüĆĒÖ®¼äÓŠČēĻĀ×Ŗ»Æ¹ŲĻµ£ŗ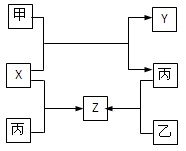
¢ÅČō¼×ŹĒ¶ĢÖÜĘŚ½šŹōµ„ÖŹ£¬ŅŅ”¢±ūŹĒ¶ĢÖÜĘŚ·Ē½šŹōµ„ÖŹ£¬X”¢Y”¢ZÖŠÖ»ÓŠŅ»ÖÖŹĒĄė×Ó¾§Ģ壬
ŹŌĶʶĻ£ŗ
¢ŁXµÄµē×ÓŹ½ŹĒ______________________________”£
¢ŚXÓė¼×·“Ó¦µÄ»Æѧ·½³ĢŹ½____________________________________”£
¢ĘČō¼×ŹĒĘųĢåµ„ÖŹ£¬±ūĶس£ŹĒŅŗĢ壬YŗĶZ¾ßÓŠĻąĶ¬µÄŃōĄė×Ó£¬XÓėZŗ¬ÓŠĻąĶ¬µÄŅõĄė×Ó£¬ŹŌĶʶĻ£ŗ
¢ŁŠ“³öZµÄ»ÆѧŹ½_______________________”£
¢ŚŠ“³öXÓė×ćĮæµÄ¼×ŌŚČÜŅŗÖŠĶźČ«·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ________________________ _ ”£
 Š”ѧ½Ģ²ÄČ«²āĻµĮŠ“š°ø
Š”ѧ½Ģ²ÄČ«²āĻµĮŠ“š°ø Š”ѧŹżŃ§æŚĖćĢāæØĶŃæŚ¶ų³öĻµĮŠ“š°ø
Š”ѧŹżŃ§æŚĖćĢāæØĶŃæŚ¶ų³öĻµĮŠ“š°ø ÓÅŠćÉśÓ¦ÓĆĢāæØæŚĖćĢģĢģĮ·ĻµĮŠ“š°ø
ÓÅŠćÉśÓ¦ÓĆĢāæØæŚĖćĢģĢģĮ·ĻµĮŠ“š°ø Õć½Ö®ŠĒæĪŹ±ÓÅ»Æ×÷ŅµĻµĮŠ“š°ø
Õć½Ö®ŠĒæĪŹ±ÓÅ»Æ×÷ŅµĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
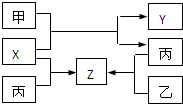 £Ø2009?½š»ŖÄ£Äā£©ČēĶ¼ĖłŹ¾£¬¼×”¢ŅŅ”¢±ūŹĒČżÖÖ³£¼ūµ„ÖŹ£¬X”¢Y”¢ZŹĒ³£¼ū»ÆŗĻĪļ£®ĖüĆĒÖ®¼äÓŠČēĻĀ×Ŗ»Æ¹ŲĻµ£ŗ
£Ø2009?½š»ŖÄ£Äā£©ČēĶ¼ĖłŹ¾£¬¼×”¢ŅŅ”¢±ūŹĒČżÖÖ³£¼ūµ„ÖŹ£¬X”¢Y”¢ZŹĒ³£¼ū»ÆŗĻĪļ£®ĖüĆĒÖ®¼äÓŠČēĻĀ×Ŗ»Æ¹ŲĻµ£ŗ
| ||
| ||
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
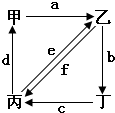 ČēĶ¼ĖłŹ¾£¬¼×”¢ŅŅ”¢±ū”¢¶”·Ö±š“ś±ķCO2”¢Na2CO3”¢NaOH”¢NaHCO3ĖÄÖÖĪļÖŹ£¬a”¢b”¢c”¢d”¢e”¢f·Ö±š±ķŹ¾Į½ÖÖĪļÖŹ¼äµÄ×Ŗ»Æ¹ŲĻµ£®¶ŌÓŚĶ¼ÖŠĮ½ÖÖĪļÖŹ¼äµÄ×Ŗ»Æ£¬ĶعżŅ»²½·“Ó¦¾ĶÄÜŹµĻÖµÄÓŠ £Ø””””£©
ČēĶ¼ĖłŹ¾£¬¼×”¢ŅŅ”¢±ū”¢¶”·Ö±š“ś±ķCO2”¢Na2CO3”¢NaOH”¢NaHCO3ĖÄÖÖĪļÖŹ£¬a”¢b”¢c”¢d”¢e”¢f·Ö±š±ķŹ¾Į½ÖÖĪļÖŹ¼äµÄ×Ŗ»Æ¹ŲĻµ£®¶ŌÓŚĶ¼ÖŠĮ½ÖÖĪļÖŹ¼äµÄ×Ŗ»Æ£¬ĶعżŅ»²½·“Ó¦¾ĶÄÜŹµĻÖµÄÓŠ £Ø””””£©²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
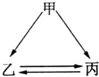 ČēĶ¼ĖłŹ¾µÄ¼×”¢ŅŅ”¢±ūČżÖÖĪļÖŹ¾łŗ¬ÓŠĻąĶ¬µÄijÖÖŌŖĖŲ£¬¼żĶ·±ķŹ¾ĪļÖŹ¼äµÄ×Ŗ»ÆŅ»²½¾ĶÄÜŹµĻÖ£¬Ōņ¼×æÉÄÜŹĒ£Ø””””£©
ČēĶ¼ĖłŹ¾µÄ¼×”¢ŅŅ”¢±ūČżÖÖĪļÖŹ¾łŗ¬ÓŠĻąĶ¬µÄijÖÖŌŖĖŲ£¬¼żĶ·±ķŹ¾ĪļÖŹ¼äµÄ×Ŗ»ÆŅ»²½¾ĶÄÜŹµĻÖ£¬Ōņ¼×æÉÄÜŹĒ£Ø””””£©| A”¢½ö¢Ł¢Ū¢Ü | B”¢½ö¢Ł¢Ś¢Ż | C”¢½ö¢Ł¢Ś¢Ū¢Ż | D”¢¢Ł¢Ś¢Ū¢Ü¢Ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
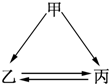 ČēĶ¼ĖłŹ¾µÄ¼×”¢ŅŅ”¢±ūČżÖÖĪļÖŹ¾łŗ¬ÓŠĻąĶ¬µÄijÖÖŌŖĖŲ£¬¼żĶ·±ķŹ¾ĪļÖŹ¼äµÄ×Ŗ»ÆŅ»²½¾ĶÄÜŹµĻÖ£¬Ōņ¼×æÉÄÜŹĒ¢ŁFe£»¢ŚHNO3£»¢ŪNa£»¢ÜC£Ø””””£©
ČēĶ¼ĖłŹ¾µÄ¼×”¢ŅŅ”¢±ūČżÖÖĪļÖŹ¾łŗ¬ÓŠĻąĶ¬µÄijÖÖŌŖĖŲ£¬¼żĶ·±ķŹ¾ĪļÖŹ¼äµÄ×Ŗ»ÆŅ»²½¾ĶÄÜŹµĻÖ£¬Ōņ¼×æÉÄÜŹĒ¢ŁFe£»¢ŚHNO3£»¢ŪNa£»¢ÜC£Ø””””£©| A”¢¢Ł¢Ś¢Ū | B”¢¢Ś¢Ū¢Ü | C”¢¢Ł¢Ś¢Ü | D”¢¢Ł¢Ś¢Ū¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
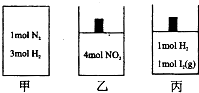 ČēĶ¼ĖłŹ¾µÄ¼×”¢ŅŅ”¢±ūČżøö¾ųČČČŻĘ÷ÖŠ·Ö±š·¢ÉśµÄ·“Ó¦ĪŖ£ŗ
ČēĶ¼ĖłŹ¾µÄ¼×”¢ŅŅ”¢±ūČżøö¾ųČČČŻĘ÷ÖŠ·Ö±š·¢ÉśµÄ·“Ó¦ĪŖ£ŗ| A”¢Čō¼×µÄĢå»żĪŖ2L£¬¾¹ż10Ćėŗó·“Ó¦“ļµ½Ę½ŗāדĢ¬£¬·Å³öČČĮæĪŖ55.44U£¬ŌņH2µÄ·“Ó¦ĖŁĀŹŹĒ0.09mol/£ØL?s£© | B”¢Čō¼×”¢ŅŅÖŠ·“Ó¦“ļµ½Ę½ŗāŹ±µÄĢå»żĻąĶ¬£¬ŌņĮ½ČŻĘ÷ÖŠĖłŗ¬ĪļÖŹµÄĮææÉÄÜĻąĶ¬ | C”¢ČōŅŅ”¢±ūÖŠ·“Ó¦“ļµ½Ę½ŗāŹ±µÄĢå»ż”¢Ń¹Ēæ¾łĻąĶ¬£¬ŌņŅŅÖŠNO2µÄ×Ŗ»ÆĀŹĪŖ50% | D”¢Čō¼×”¢ŅŅ”¢±ūÖŠ·“Ó¦¾ł“ļµ½Ę½ŗāדĢ¬Ź±£¬Ōņ¼×ÖŠĪļÖŹµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæ²»±ä£¬ŅŅÖŠĪļÖŹµÄŃÕÉ«²»±ä£¬±ūÖŠµÄĪĀ¶Č²»±ä |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com