
【题目】在试管A中先加入46 g CH3CH2OH,边摇动边缓缓加入2 mL浓硫酸并充分摇匀,冷却后再加入30 g CH3COOH,充分混合后将试管固定在铁架台上,在试管B中加入7mL C溶液。连接好装置用酒精灯对试管A加热,当观察到试管B中有明显现象时停止加热。
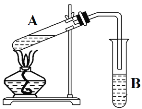
(1)浓硫酸的作用是__________
(2)B装置中观察到的现象是______
(3)溶液C为_________, B中导管未插入液面以下,其原因是__________
A 饱和NaOH溶液 b 水 c 饱和Na2CO3溶液d CCl4
(4)最后通过分离提纯得到乙酸乙酯 30.8 g ,则乙酸乙酯的实际产率是____(实际产率 = ![]() ×100%)
×100%)
【答案】催化剂 吸水剂 溶液分层,液面上有无色透明的不溶于水的油状液体产生 c 防止倒吸 70%
【解析】
该实验装置是实验室制取乙酸乙酯的实验装置,反应为CH3COOH+CH3CH2OH![]() CH3COOC2H5+H2O,实验中,为防止浓硫酸加入水中放热,造成液体飞溅引发实验安全,药品的添加顺序为:在试管A中先加入46 g CH3CH2OH,边摇动边缓缓加入2 mL浓硫酸并充分摇匀,冷却后再加入30 g CH3COOH,充分混合后将试管固定在铁架台上,加热制取乙酸乙酯,一段时间后在B试管液面上产生无色透明油状液体,即为乙酸乙酯,据此分析解答。
CH3COOC2H5+H2O,实验中,为防止浓硫酸加入水中放热,造成液体飞溅引发实验安全,药品的添加顺序为:在试管A中先加入46 g CH3CH2OH,边摇动边缓缓加入2 mL浓硫酸并充分摇匀,冷却后再加入30 g CH3COOH,充分混合后将试管固定在铁架台上,加热制取乙酸乙酯,一段时间后在B试管液面上产生无色透明油状液体,即为乙酸乙酯,据此分析解答。
(1)浓硫酸在制取乙酸乙酯的实验中的催化剂和吸水剂;
(2)生成的乙酸乙酯在水溶液上层,试管中观察到的现象是:溶液分层,液面上有无色透明的不溶于水的油状液体产生;
(3)实验中使用的乙酸和乙醇都具有挥发性,加热条件可加速二者挥发,则制得的乙酸乙酯中混有乙酸和乙醇,应使用饱和碳酸钠溶液,既可以除去乙酸,还能溶解乙醇;为防止乙酸和乙醇两种蒸气被吸收而引起倒吸现象,B装置中的导管不能插入液面以下;
(4)46 g CH3CH2OH的物质的量为![]() =1mol,30 g CH3COOH的物质的量为
=1mol,30 g CH3COOH的物质的量为![]() =0.5mol,制取乙酸乙酯的反应为CH3COOH+CH3CH2OH
=0.5mol,制取乙酸乙酯的反应为CH3COOH+CH3CH2OH![]() CH3COOC2H5+H2O,则乙醇过量,用乙酸的量计算,理论上乙酸完全参与反应生成乙酸乙酯的物质的量为0.5mol,则质量为0.5mol×88g/mol=44g,最后通过分离提纯得到乙酸乙酯 30.8 g ,则乙酸乙酯的实际产率是=
CH3COOC2H5+H2O,则乙醇过量,用乙酸的量计算,理论上乙酸完全参与反应生成乙酸乙酯的物质的量为0.5mol,则质量为0.5mol×88g/mol=44g,最后通过分离提纯得到乙酸乙酯 30.8 g ,则乙酸乙酯的实际产率是= ![]() ×100%=
×100%=![]() ×100%=70%。
×100%=70%。


科目:高中化学 来源: 题型:
【题目】锌在工业中有重要作用,也是人体必需的微量元素。回答下列问题:
(1)Zn原子核外电子排布式为 _________________________________。
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能I1(Zn)________I1(Cu)(填“大于”或“小于”)。原因是______________________。
(3)ZnF2具有较高的熔点(872 ℃),其化学键类型是________;ZnF2不溶于有机溶剂而ZnCl2、ZnBr2、ZnI2能够溶于乙醇、乙醚等有机溶剂,原因是______________________。
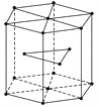
(4)金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为____________________。六棱柱底边边长为acm,高为ccm,阿伏加德罗常数的值为NA,Zn的密度为________g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为研究铜与浓硫酸的反应,某化学兴趣小组进行如下实验。
实验I:反应产物的定性探究,按如图装置(固定装置已略去)进行实验:
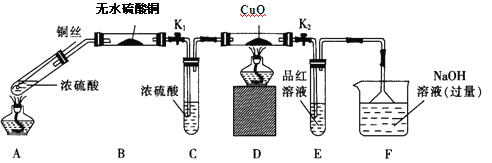
(1)F装置的烧杯中发生反应的离子方程式是_____________;B装置中的现象是__________。
(2)实验过程中,能证明浓硫酸中硫元素的氧化性强于氢元素的现象是_________。
(3)实验结束时,撤去所有酒精灯之前必须完成的实验操作是_________。
(4)实验结束后,证明A装置试管中反应所得产物是否含有铜离子的操作方法是_________。
实验Ⅱ:反应产物的定量探究
(5)在铜与浓硫酸反应的过程中,发现有黑色物质出现,且黑色物质为Cu2S。产生Cu2S的反应为aCu+bH2SO4=cCu2S+dCuSO4+eH2O,则a∶b=______
(6)为测定硫酸铜的产率,将该反应所得溶液中和后配制成250.00 mL溶液,取该溶液25.00 mL加入足量 KI溶液中振荡,以淀粉溶液为指示剂,用0.36 mol·L-1的Na2S2O3溶液滴定生成的I2,3次实验平均消耗该Na2S2O3溶液25.00 mL。若反应消耗铜的质量为6.4 g,则硫酸铜的产率为___。
(已知![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】六苯乙烷为无色晶体,其结构如图所示。下列有关说法中正确的是( )
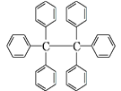
A. 它是一种苯的同系物,易溶于有机溶剂中
B. 它的分子式为C38H30,只含有非极性键
C. 它的分子中所有原子共平面
D. 核磁共振氢谱有3组峰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某有机物A的红外光谱和核磁共振氢谱图如下图所示,下列说法中不正确的是( )
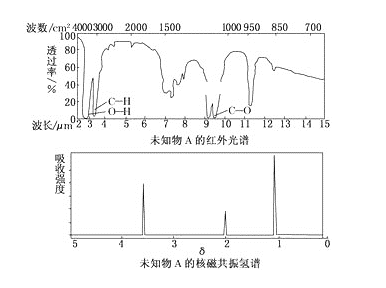
A. 由红外光谱可知,该有机物中至少有三种不同的化学键
B. 由核磁共振氢谱图可知,该有机物分子中有三种不同的氢原子
C. 仅由其核磁共振氢谱图无法得知其分子中的氢原子总数
D. 若A的化学式为C2H6O,则其结构简式为CH3—O—CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学欲证明乙炔能与KMnO4酸性溶液反应,实验方案如下:将电石与水反应生成的气体通入KMnO4酸性溶液,溶液褪色,证明二者发生了反应。请回答:
(1)制备乙炔的反应的化学方程式是_______。
(2)该同学的实验方案存在的问题是______。
(3)为了解决上述问题,需重新选择实验装置,备选装置如图所示。
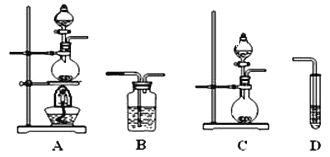
①将装置编号按顺序填在横线上___→B→__________。
②B装置中所盛放的试剂是____________。
(4)乙炔使酸性KMnO4溶液褪色的离子方程式是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:原子序数小于18的同一主族的两种元素X和Y,其原子半径:X<Y。下列说法正确的是
A. 若X和Y均位于VIIA,则键能大小为HX<HY
B. 若X和Y均位于VIA,则H2X分子间易形成氢键
C. 若X和Y均位于IVA,则二者最高价氧化物的晶体类型相同
D. 若X和Y均位于IIA,则第一电离能大小为X<Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着科学技术的发展和环保要求的不断提高,CO2的捕集利用技术成为研究的重点。完成下列填空:
(1)目前国际空间站处理CO2的一个重要方法是将CO2还原,所涉及的反应方程式为:CO2(g)+4H2(g)![]() CH4(g)+2H2O(g),已知H2的体积分数随温度的升高而增加.若温度从300℃升至400℃,重新达到平衡,判断下列表格中各物理量的变化。(选填“增大”、“减小”或“不变”)
CH4(g)+2H2O(g),已知H2的体积分数随温度的升高而增加.若温度从300℃升至400℃,重新达到平衡,判断下列表格中各物理量的变化。(选填“增大”、“减小”或“不变”)
v正 | v逆 | 平衡常数K | 转化率α |
________ | ________ | ________ | ________ |
(2)相同温度时,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如下表:
[CO2]/molL﹣1 | [H2]/molL﹣1 | [CH4]/molL﹣1 | [H2O]/molL﹣1 | |
平衡Ⅰ | a | b | c | d |
平衡Ⅱ | m | n | x | y |
a、b、c、d与m、n、x、y之间的关系式为________.
(3)碳酸:H2CO3 , K1=4.3×10﹣7 , K2=5.6×10﹣11 草酸:H2C2O4 , K1=5.9×10﹣2 , K2=6.4×10﹣5 ,0.1mol/LNa2CO3溶液的pH____0.1mol/LNa2C2O4溶液的pH,(选填“大于”“小于”或“等于”),等浓度的草酸溶液和碳酸溶液中,氢离子浓度较大的是___.
(4)在如图的转化关系中(X代表卤素)。ΔH2_____0(填“>”、“=”或“<”);△H1、△H2和△H3三者存在的关系为_______。
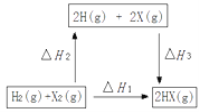
(5)现有浓度均为0.1mol·L-1的下列溶液:①硫酸、②醋酸、③氢氧化钠、④醋酸钠。请回答下列问题:
①醋酸钠中各离子浓度由大到小的顺序是_______。
②醋酸和醋酸钠等体积混合所得溶液中:c(CH3COOH)+c(CH3COO-)=______mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)写出下列物质的电子式:Na2O2_____NH3_____。
(2)2.2g铵根14N2H4+的中子数是___,核外电子数是____,某微粒含有一个原子核,核中有 17个质子,20个中子,核外有 18个电子,该粒子的化学符号是____。
(3)已知断开 1mol H—H 键、1mol I—I 键、1mol H—I 键分别需要吸收的能量为 436kJ、151kJ、299kJ,则由 1mol H2和 1mol I2生成 2mol HI会_____(“放出”或“吸收”)_____kJ 的热量。
(4)现有下列物质:①H2 ②Na2O2 ③NaOH ④H2O2 ⑤CaCl2 ⑥NH4NO3 ⑦H2S,只由离子键构成的物质是_____(填序号,同下),由离子键和共价键构成的物质是_________,属于共价化合物的是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com