
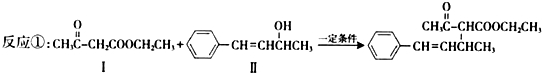
 .
.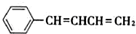 .
.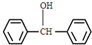 与
与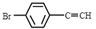 ,也可以发生类似反应①的反应,有机产物的结构简式为
,也可以发生类似反应①的反应,有机产物的结构简式为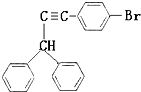 .
. 分析 (1)化合物I的结构简式为CH3COCH2COOCH2CH3,根据结构简式可得分子式,写出反应的方程式可得耗氧量;
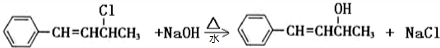
(2)化合物Ⅱ的官能团是碳碳双键、羟基,前者与溴可以发生加成反应,前者和后者都能被酸性高锰酸钾溶液氧化,由此推断化合物Ⅱ可以使溴的四氯化碳溶液或溴水或酸性高锰酸钾溶液褪色;化合物Ⅲ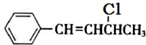 可生成化合物Ⅱ,发生卤代烃的水解反应;
可生成化合物Ⅱ,发生卤代烃的水解反应;
(3)化合物Ⅲ与NaOH乙醇溶液共热生成的有机产物可能是C6H5CH=C=CHCH3、C6H5CH=CHCH=CH2,Ⅳ的核磁共振氢谱除苯环峰外还有四组峰,峰面积之比为1:1:1:2,则化合物IV的结构简式为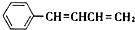 ;
;
(4)醇中羟-CH2OH在Cu催化下与过量O2反应生成能发生银镜反应的醛基(-CHO),可知V的碳链两端各有1个-CH2OH,CH3COOCH2CH3的分子式为C4H8O2,减去2个C、6个H、2个O之后可得2个C、2个H,即V的碳链中间剩余基团为-CH=CH-,则V的结构简式为HOCH2CH=CHCH2OH,可以推断VI的结构简式为OHCCH=CHCHO;
(5)比较反应①中反应物I、Ⅱ与生成物的结构简式,该反应实质是Ⅱ所含醇羟基中氧碳键断裂,I所含酯基和酮基的邻碳上的碳氢键断裂,羟基与氢结合生成无机产物水,其余部分结合生成有机产物.
解答 解:(1)化合物I的结构简式为CH3COCH2COOCH2CH3,其分子式为C6H10O3,燃烧方程式为:C6H10O3+7O2$\stackrel{点燃}{→}$6CO2+5H2O,则1mol I完全燃烧最少需要消耗7mol O2,
故答案为:C6H10O3; 7;
(2)化合物Ⅱ的官能团是碳碳双键、羟基,前者与溴可以发生加成反应,前者和后者都能被酸性高锰酸钾溶液氧化,化合物Ⅲ的结构简式为C6H5CH=CHCHClCH3,与NaOH在加热条件下发生水解反应生成Ⅱ,反应的方程式为 ,
,
故答案为:溴水或酸性高锰酸钾; ;
;
(3)化合物Ⅲ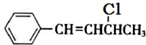 与NaOH乙醇溶液共热生成的有机产物可能是C6H5CH=C=CHCH3、C6H5CH=CHCH=CH2,Ⅳ的核磁共振氢谱除苯环峰外还有四组峰,峰面积之比为为1:1:1:2,化合物IV的结构简式为
与NaOH乙醇溶液共热生成的有机产物可能是C6H5CH=C=CHCH3、C6H5CH=CHCH=CH2,Ⅳ的核磁共振氢谱除苯环峰外还有四组峰,峰面积之比为为1:1:1:2,化合物IV的结构简式为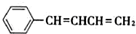 ,
,
故答案为: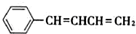 ;
;
(4)醇中羟-CH2OH在Cu催化下与过量O2反应生成能发生银镜反应的醛基(-CHO),可知V的碳链两端各有1个-CH2OH,CH3COOCH2CH3的分子式为C4H8O2,减去2个C、6个H、2个O之后可得2个C、2个H,即V的碳链中间剩余基团为-CH=CH-,则V的结构简式为HOCH2CH=CHCH2OH,可以推断VI的结构简式为OHCCH=CHCHO,
故答案为:HOCH2CH=CHCH2OH;OHCCH=CHCHO;
(5)比较反应①中反应物I、Ⅱ与生成物的结构简式,该反应实质是Ⅱ所含醇羟基中氧碳键断裂,I所含酯基和酮基的邻碳上的碳氢键断裂,羟基与氢结合生成无机产物水,其余部分结合生成有机产物,则 与
与 发生类似反应①的反应生成有机产物的结构简式为
发生类似反应①的反应生成有机产物的结构简式为 ,
,
故答案为: .
.
点评 本题考查有机物的推断与合成,综合考查考生的分析能力、逻辑推理能力、综合应用信息以及信息迁移能力,是对有机化学基础的综合考查.


科目:高中化学 来源: 题型:实验题
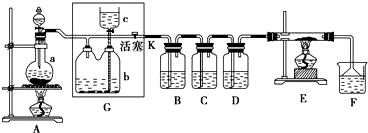
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 绿色食品就是不含任何化学物质的食品 | |
| B. | 燃煤时添加生石灰以减少SO2的排放 | |
| C. | PM2.5是指环境空气中直径小于或等于2.5微米的颗粒物 | |
| D. | pH在5.6~7.0之间的降水通常称为酸雨 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 )具有高度的对称性,Eaton教授在此基础上经七步反应合成了二羧基立方烷,二羧基立方烷的同分异构体数目为( )
)具有高度的对称性,Eaton教授在此基础上经七步反应合成了二羧基立方烷,二羧基立方烷的同分异构体数目为( )| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
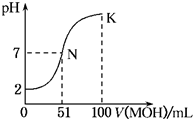 常温下,向100mL 0.01mol•L-1HA溶液中逐滴加入0.02mol•L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).回答下列问题:
常温下,向100mL 0.01mol•L-1HA溶液中逐滴加入0.02mol•L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 脱氧过程是吸热反映,可降低温度,延长糕点保质期 | |
| B. | 脱氧过程中铁作原电池负极,电极反应为:Fe-3e-→Fe3+ | |
| C. | 脱氧过程中热能转化为生成物的内部能量 | |
| D. | 标准状况能吸收氧气336mL,理论上最少要含有1.12g铁粉的脱氧剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;X在UW2中剧烈燃烧生成的黑、白两种固体中化学键类型依次是共价键、离子键.
;X在UW2中剧烈燃烧生成的黑、白两种固体中化学键类型依次是共价键、离子键.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com