
【题目】铵明矾[NH4Al(SO4)2·12H2O]是分析化学常用的基准试剂,工业上常用铝土矿(主要成分为Al2O3)来生产铵明矾,其中Z的水溶液可用于伤口消毒,其工艺流程图如下:
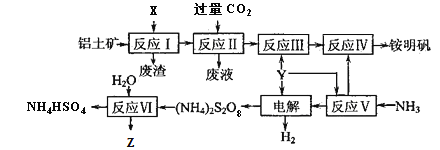
(1)写出反应Ⅱ的离子方程式____________________。
(2)25℃时,将0.2 mol·L-1的氨水与0.1 mol·L-1的Y溶液等体积混合,所得溶液的pH=5,则该温度下氨水的电离常数Kb≈_____________(忽略混合时溶液体积的变化)。
(3)从反应Ⅳ的铵明矾溶液中获得铵明矾晶体的实验操作依次为_____________、____________、过滤、洗涤(填操作名称)。
(4)“电解”时,用惰性材料作电极,则阳极电极反应式为__________________________。
(5)反应Ⅵ的化学方程式为______________________。
(6)废水中含有Fe2+、Mn2+等金属离子对自然环境有严重的破坏作用,,可用(NH4)2S2O8氧化除去。写出Mn2+被氧化生成MnO2的离子方程式为__________________________________。Z也有较强氧化性,在实际生产中不用Z氧化Mn2+的原因是_______________________________________。
【答案】 AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- 1×10-5 蒸发浓缩 冷却结晶 2SO42-—2e-= S2O82- (NH4)2S2O8+2H2O = 2NH4HSO4+H2O2 S2O82- + 2H2O + Mn 2+=4H+ + 2SO42- + MnO2↓ 锰的化合物可催化H2O2的分解,使消耗的H2O2增多
【解析】(1)氧化铝与强碱溶液反应生成偏铝酸盐溶液,向溶液中通入足量二氧化碳气体生成氢氧化铝和碳酸氢盐,离子方程式AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;正确答案:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-。
(2)根据题意可知,设溶液的体积均为1L,氨水和硫酸恰好完全反应生成硫酸铵0.1mol,根据水解反应NH4++H2O![]() NH3H2O+H+可知:所得溶液的pH=5,c(H+)=10-5mol/L, c(NH3H2O)= 10-5mol/L, 两溶液等体积混合,所以c(NH4+)=0.1 mol/L,根据水解平衡常数计算公式可得:Kh=KW/Kb= c(NH3H2O) ×c(H+)/ c(NH4+), KW=10-14,所以带入数值后得Kb≈1×10-5;正确答案:1×10-5。
NH3H2O+H+可知:所得溶液的pH=5,c(H+)=10-5mol/L, c(NH3H2O)= 10-5mol/L, 两溶液等体积混合,所以c(NH4+)=0.1 mol/L,根据水解平衡常数计算公式可得:Kh=KW/Kb= c(NH3H2O) ×c(H+)/ c(NH4+), KW=10-14,所以带入数值后得Kb≈1×10-5;正确答案:1×10-5。
(3)先把铵明矾水溶液进行蒸发浓缩 ,再降温结晶,过滤、洗涤,得到该物质的晶体,实验操作依次为蒸发浓缩 、冷却结晶; 正确答案:蒸发浓缩 、冷却结晶。
(4)有反应III可知,氢氧化铝溶于硫酸溶液生成硫酸铝,所以试剂Y为硫酸溶液,通过流程看出,溶液中的氢离子得电子变为氢气,那么只有硫酸根离子失电子变为S2O82-,则阳极电极反应式为2SO42-—2e-= S2O82-;正确答案:2SO42-—2e-= S2O82-。
(5)根据流程图看出,(NH4)2S2O8与水反应生成NH4HSO4,再根据原子守恒规律,得另外一种物质为H2O2,反应Ⅵ的化学方程式为(NH4)2S2O8+2H2O = 2NH4HSO4+H2O2 ;正确答案:(NH4)2S2O8+2H2O = 2NH4HSO4+H 2O2。
(6)根据氧化还原反应规律:Mn2+被氧化生成MnO2,S2O82-被还原为SO42-,根据电子守恒、电荷守恒、原子守恒写出离子方程式为S2O82- + 2H2O + Mn 2+=4H+ + 2SO42- + MnO2↓;正确答案:S2O82- + 2H2O + Mn 2+=4H+ + 2SO42- + MnO2↓。过氧化氢也有较强氧化性,但在实际生产中不用Z氧化Mn2+,原因是锰的化合物可催化H2O2的分解,使消耗的H2O2增多;正确答案:锰的化合物可催化H2O2的分解,使消耗的H2O2增多。


科目:高中化学 来源: 题型:
【题目】固体碘化铵置于密闭容器中,加热至一定温度后恒温;容器中发生反应:①NH4I(s)![]() NH3(g)+HI(g)②2HI(g)
NH3(g)+HI(g)②2HI(g)![]() H2(g)+I2(g),测得平衡时c(H2)=0.5mol/L,反应①的平衡常数为20,则下列结论正确的是 ( )
H2(g)+I2(g),测得平衡时c(H2)=0.5mol/L,反应①的平衡常数为20,则下列结论正确的是 ( )
A. 平衡时HI分解率为20%
B. 当固体碘化铵物质的量增大一倍,则在相同条件下,容器内压强变大
C. 固体碘化铵一定完全分解
D. 平衡时C(HI)=5mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组探究铁和硝酸银溶液的反应,实验过程如下:
实验序号 | 实验操作 | 实验现象 |
I | 将一束光亮洁净的铁丝伸入到0.1mol/L 的AgNO3溶液中 | 铁丝表面有银白色固体析出,溶液逐渐变为浅绿色 |
II | 取少量实验I中上层清液,滴入K3[Fe(CN) 6]溶液 | 有蓝色沉淀生成 |
(1)根据上述实验现象,甲同学认为有Fe2+生成,铁和硝酸银溶液的反应的离子方程式是____________________。
(2)乙同学认为实验中可能生成Fe3+,设计并完成如下实验
实验序号 | 实验操作 | 实验现象 |
III | 取少量实验I中上层清液,滴入少量KSCN溶液,振荡 | 产生白色沉淀,溶液局部变红,振荡后红色消失,沉淀量增加 |
查阅资料:Ag+与SCN-生成白色沉淀AgSCN
乙同学判断有Fe3+,理由是 ____________________。
(3)乙同学继续探究红色褪去的原因,设计并完成如下实验
实验序号 | 实验操作 | 实验现象 |
IV | 取少量实验I中上层清液,滴加几滴稀盐酸 | 有白色沉淀生成 |
V | 取1mLFe(NO3)3溶液,滴加2滴等浓度的KSCN溶液,振荡,再滴加少量AgNO3溶液 | 溶液变红;振荡溶液颜色无变化,滴加AgNO3后溶液红色褪去,产生白色沉淀. |
① 实验IV的目的是____________________;
② 用平衡移动原理解释,实验V中溶液红色褪去的原因____________________。
(4)丙认为溶液中Fe3+是Fe2+被Ag+氧化所致。按下图连接装置并进行实验,一段时间后取出左侧烧杯溶液加入KSCN溶液,溶液变红
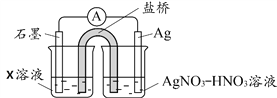
① 其中X溶液是____________________;
② 由实验得出Ag+和Fe2+反应的离子方程式是____________________;
③ 丙同学的实验设计及结论是否合理,请说明理由____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为:CH3CH2OH﹣4e﹣+H2O=CH3COOH+4H+ . 下列说法中正确的是( )
A.正极上发生的反应为:O2+2H2O+4e﹣=4OH﹣
B.电池反应的化学方程式为:CH3CH2OH+O2=CH3COOH+H2O
C.检测时,溶液中的H+向负极移动
D.若有0.4mol电子转移,则在标准状况下消耗4.48L氧气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中蕴藏着丰富的资源,海水综合利用的流程图如图1: 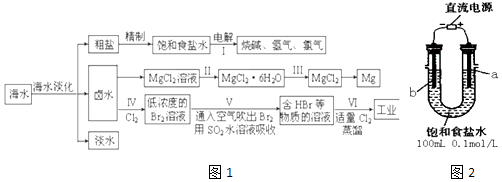
(一)某化学研究小组用图装置2模拟步骤I电解食盐水 (用铁和石墨做电极).
(1)a电极材料是(填铁、石墨),其电极反应式为 .
(2)当阴极产生11.2mL气体时(标准状况),该溶液的pH为(忽略反应前后溶液体积的变化). (二)卤水中蕴含着丰富的镁资源,就MgCl2粗产品的提纯、镁的冶炼过程回答下列问题:已知MgCl2粗产品的溶液中含有Fe2+、Fe3+和Al3+ . 表是生成氢氧化物沉淀的pH:
物质 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Mg(OH)2 |
开始沉淀pH | 2.7 | 8.1 | 3.8 | 9.5 |
完全沉淀pH | 3.7 | 9.6 | 4.8 | 11.0 |
(3)把MgCl2粗产品的溶液中的Fe2+转化为Fe3+ , 最适宜选用的物质是(填序号,下同),加入调节溶液的pH,充分反应后过滤,可得MgCl2溶液. a.KMnO4 b.H2O2 c.MgO d.NaOH
(4)步骤Ⅲ由MgCl2H2O获得MgCl2的操作是: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁、钴、铜是重要的过渡元素,其化合物具有广泛的用途。
(1)钴位于元素周期表中第____族,基态Cu的核外电子排布式是_________。元素铁与铜的第二电离能分别为:ICu=1958kJ/mol、IFe=1561kJ/mol,ICu>IFe的原因是______________。
(2)有机铁肥三硝酸六尿素合铁(Ⅲ),化学式为:[Fe(H2NCONH2)6](NO3)3.
①尿素分子中C原子的杂化方式是_______,所含非金属元素的电负性由大到小的顺序是_____。
②[Fe(H2NCONH2)6](NO3)3中“H2NCONH2”与Fe(Ⅲ)之间的作用力是_______。根据价层电子对互斥理论推测NO3-的空间构型为_________。
(3)Fe3+可用SCN-检验,其对应的酸有两种,分别为硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S),这两种酸中沸点较高的是________________,原因是________________。
(4)FeCl3晶体易溶于水喝乙醇,用酒精灯加热即可气化,由此可知FeCl3的晶体类型为_____;S和Fe形成的某化合物,其晶胞如图一所示,则该物质的化学式为_______。

(5)Cu晶体的堆积方式如图二所示,晶体中Cu原子的配位数为_______;设Cu原子半径为a,晶体空间利用率为_______(用含a的式子表达,不化简)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国稀土资源丰富,下列有关稀土元素![]() Sm与
Sm与![]() Sm的说法正确的是( )
Sm的说法正确的是( )
A. 通过化学变化可实现![]() Sm与
Sm与![]() Sm的相互转化
Sm的相互转化
B. ![]() Sm与
Sm与![]() Sm的核外电子排布方式相同
Sm的核外电子排布方式相同
C. Sm元素的近似相对原子质量为150
D. ![]() Sm与
Sm与![]() Sm核外电子数和中子数均为62
Sm核外电子数和中子数均为62
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,pH=l 的某溶液 A 中除H+外,还含有NH4+、K+、Na+、Fe3+、Al3+、Fe2+、CO32-、NO3-、 Cl-、I-、SO42-中的4种,且溶液中各离子的物质的量浓度均为0.1mol·L-1。现取该溶液进行有关实验,实验结果如下图所示,下列有关说法正确的是

A. 该溶液中一定有上述离子中的NO3-、Al3+、SO42-、Cl-四种离子
B. 实物消耗Cu14.4g,则生成气体丁的体积为3.36L
C. 该溶液一定没有Fe3+,但是无法确定是否含有I-
D. 沉淀乙一定有BaCO3,可能有BaSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组同学通过下列流程制取不溶于水和稀硫酸的黄钾铵铁矾1KNH4Fex(OH)y(SO4)z],并通过实验测定样品中黄钾铵铁矾的有关组成. 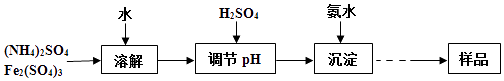
实验测定:
①称取一定质量的样品加入稀盐酸中充分溶解,将所得溶液转移至容量瓶并配制成l00mL溶液A;
②量取25.00mL溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体4.66g;
③量取25.00mL溶液A,加入足量KI,用1.000molL﹣1Na2S2O3溶液进行滴定(已知反应为I2+2Na2S2O3═2NaI+Na2S4O6),消耗30.00mL Na2S2O3溶液至终点.
(1)在1KNH4Fex(OH)y(SO4)z]中x、y、z的代数关系式为 .
(2)过滤所需要的主要玻璃仪器有、、 .
(3)写出实验测定③中加入足量KI反应的离子方程式 .
(4)根据以上实验数据计算样品中的n(SO42﹣):n(Fe3+).(写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com