
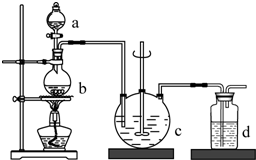
 ¹ĢĢåŃõ»ÆĪļČ¼ĮĻµē³ŲŹĒÓÉĆĄ¹śĪ÷ĪŻ£ØWestinghouse£©¹«Ė¾ŃŠÖĘæŖ·¢µÄ£®ĖüŅŌ¹ĢĢåŃõ»ÆļÆ-Ńõ»ÆīĘĪŖµē½āÖŹ£¬ÕāÖÖ¹ĢĢåµē½āÖŹŌŚøßĪĀĻĀŌŹŠķŃõĄė×Ó£ØO2-£©ŌŚĘä¼äĶعż£®øƵē³ŲµÄ¹¤×÷ŌĄķČēĶ¼ĖłŹ¾£¬ĘäÖŠ¶ąæ×µē¼«a”¢b¾ł²»²ĪÓėµē¼«·“Ó¦£®ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ£Ø””””£©
¹ĢĢåŃõ»ÆĪļČ¼ĮĻµē³ŲŹĒÓÉĆĄ¹śĪ÷ĪŻ£ØWestinghouse£©¹«Ė¾ŃŠÖĘæŖ·¢µÄ£®ĖüŅŌ¹ĢĢåŃõ»ÆļÆ-Ńõ»ÆīĘĪŖµē½āÖŹ£¬ÕāÖÖ¹ĢĢåµē½āÖŹŌŚøßĪĀĻĀŌŹŠķŃõĄė×Ó£ØO2-£©ŌŚĘä¼äĶعż£®øƵē³ŲµÄ¹¤×÷ŌĄķČēĶ¼ĖłŹ¾£¬ĘäÖŠ¶ąæ×µē¼«a”¢b¾ł²»²ĪÓėµē¼«·“Ó¦£®ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ£Ø””””£©| A£® | ÓŠO2²Ī¼Ó·“Ó¦µÄa¼«ĪŖµē³ŲµÄøŗ¼« | |
| B£® | ÓŠH2²Ī¼Ó·“Ó¦µÄb¼«ĪŖµē³ŲµÄÕż¼« | |
| C£® | a¼«¶ŌÓ¦µÄµē¼«·“Ó¦Ź½ĪŖO2+2H2O-4eØT4OH- | |
| D£® | øƵē³ŲµÄ×Ü·“Ó¦·½³ĢŹ½ĪŖ£ŗ2H2+O2ØT2H2O |
·ÖĪö øƵē³ŲŹōÓŚ¹ĢĢåČ¼ĮĻµē³Ų£¬ŅŌ¹ĢĢåŃõ»ÆļÆ-Ńõ»ÆīĘĪŖµē½āÖŹ£¬µē³Ų¹¤×÷Ź±£¬Õż¼«ÉĻŃõĘųµĆµē×ÓÉś³ÉŃõĄė×Ó£¬ŌņÕż¼«ÉĻ·“Ó¦ĪŖO2+4e-=2O2-£»øŗ¼«ĪŖĒāĘųŹ§µē×Ó·¢ÉśŃõ»Æ·“Ó¦£¬øŗ¼«·“Ó¦ĪŖ£ŗ2H2-4e-+2O2-ØT2H2O£¬×Ü·“Ó¦ĪŖ£ŗ2H2+O2$\frac{\underline{\;øßĪĀ\;}}{\;}$2H2O£®
½ā“š ½ā£ŗA”¢ŌŚČ¼ĮĻµē³ŲÖŠ£¬ÓŠO2²Ī¼ÓµÄa¼«ĪŖŌµē³ŲµÄÕż¼«£¬¹ŹA“ķĪó£»
B”¢ÓŠĒāĘų²Ī¼Ó·“Ó¦µÄµē¼«ĪŖøŗ¼«£¬¹ŹB“ķĪó£»
C”¢a¼«ĪŖÕż¼«£¬µē¼«·“Ó¦ĪŖ£ŗO2+4e-=2O2-£¬¹ŹC“ķĪó£»
D”¢øƵē³ŲµÄ×Ü·“Ó¦Ź½ĪŖ2H2+O2$\frac{\underline{\;øßĪĀ\;}}{\;}$2H2O£¬¹ŹDÕżČ·£»
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²éŌµē³ŲµÄ¹¤×÷ŌĄķ£¬Éę¼°Õżøŗ¼«µÄÅŠ¶Ļ£¬µē¼«·“Ó¦Ź½µÄŹéŠ“µČĪŹĢā£¬ĢāÄæÄŃ¶Č²»“ó£¬×¢Ņā»ł“”ÖŖŹ¶µÄ»żĄŪ£®


 ŠĀæĪ±ź½×ĢŻŌĶĮѵĮ·ĻµĮŠ“š°ø
ŠĀæĪ±ź½×ĢŻŌĶĮѵĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 Įņ“śĮņĖįÄĘ£ØNa2S2O3£©£¬Ė×Ćūŗ£²Ø”¢“óĖÕ“ņ£®Ķس£ĪŖĪŽÉ«¾§Ģ壬Ņ×ČÜÓŚĖ®£¬ÄŃČÜÓŚ¾Ę¾«£¬ŹÜČČ”¢ÓöĖįŅ×·Ö½ā£®Ņ½Ń§ÉĻÓĆÓŚĒĄ¾ČĒč»ÆĪļÖŠ¶¾£¬³£ÓĆÓŚµā»Æ·ØµÄ²āĮ森¹¤ŅµÖʱøµÄ·“Ó¦ŌĄķĪŖ£ŗ2Na2S+Na2CO3+4SO2ØT3Na2S2O3+CO2£¬ŹµŃéŹŅÄ£ÄāøĆ¹¤Ņµ¹ż³ĢµÄ×°ÖĆČēĶ¼ĖłŹ¾£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
Įņ“śĮņĖįÄĘ£ØNa2S2O3£©£¬Ė×Ćūŗ£²Ø”¢“óĖÕ“ņ£®Ķس£ĪŖĪŽÉ«¾§Ģ壬Ņ×ČÜÓŚĖ®£¬ÄŃČÜÓŚ¾Ę¾«£¬ŹÜČČ”¢ÓöĖįŅ×·Ö½ā£®Ņ½Ń§ÉĻÓĆÓŚĒĄ¾ČĒč»ÆĪļÖŠ¶¾£¬³£ÓĆÓŚµā»Æ·ØµÄ²āĮ森¹¤ŅµÖʱøµÄ·“Ó¦ŌĄķĪŖ£ŗ2Na2S+Na2CO3+4SO2ØT3Na2S2O3+CO2£¬ŹµŃéŹŅÄ£ÄāøĆ¹¤Ņµ¹ż³ĢµÄ×°ÖĆČēĶ¼ĖłŹ¾£¬»Ų“šĻĀĮŠĪŹĢā£ŗ| ŹµŃéŠņŗÅ | 1 | 2 | 3 |
| Na2S2O3ČÜŅŗĢå»ż£ØmL£© | 19.98 | 20.02 | 21.18 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĻņCa£ØClO£©2ČÜŅŗÖŠĶØČėÉŁĮæSO2Ca2++3ClO-+SO2+H2OØTCaSO4”ż+Cl-+2HClO | |
| B£® | 1mol/LµÄNaAlO2ČÜŅŗŗĶ2.5mol/LµÄŃĪĖįµČĢå»ż¾łŌČ»ģŗĻ£ŗ2AlO2-+5H+ØTAl£ØOH£©3”ż+Al3++H2O | |
| C£® | ½«11.2L±ź×¼×“æöĻĀµÄĀČĘųĶØČė200mL2mol/LµÄFeBr2ČÜŅŗÖŠ£¬Ąė×Ó·“Ó¦·½³ĢŹ½ĪŖ£ŗ2Fe2++8Br-+5Cl2ØT2Fe3++4Br2+10Cl- | |
| D£® | ĻņNH4HCO3ČÜŅŗÖŠ¼ÓČė×ćĮæNaAlO2ČÜŅŗ£ŗNH4++2AlO2-+HCO3--+2H2OØTNH3”ü+2Al£ØOH£©3”ż+CO32-£® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
| ĪļÖŹ | ČŪµć/”ę | ·Šµć/”ę | ĘäĖüŠŌÖŹ |
| SO2Cl2 | -54.1 | 69.1 | ¢ŁŅ×Ė®½ā£¬²śÉś“óĮæ°×Īķ ¢ŚŅ×·Ö½ā£ŗSO2Cl2$\frac{\underline{\;100”ę\;}}{\;}$ SO2”ü+Cl2”ü |
| H2SO4 | 10.4 | 338 | ĪüĖ®ŠŌĒŅ²»Ņ×·Ö½ā |

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
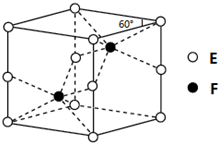 A”¢B”¢C”¢D”¢E”¢FĪŖŌŖĖŲÖÜĘŚ±ķĒ°ĖÄÖÜĘŚµÄŌŖĖŲ£¬Ō×ÓŠņŹżŅĄ“ĪŌö“ó£®AŌŖĖŲµÄµ„ÖŹŹĒæÕĘųµÄÖ÷ŅŖ³É·Ö£¬BŌ×ÓŗĖĶāp¹ģµĄÉĻÓŠ1¶Ō³É¶Ōµē×Ó£¬DŌŖĖŲµÄ¼Ūµē×ÓŹżŹĒĘäÓąµē×ÓŹżµÄŅ»°ė£¬CÓėBĶ¬Ö÷×壬AÓėFĶ¬Ö÷×壬DÓėEĶ¬×壮»Ų“šĻĀĮŠĪŹĢā£ŗ
A”¢B”¢C”¢D”¢E”¢FĪŖŌŖĖŲÖÜĘŚ±ķĒ°ĖÄÖÜĘŚµÄŌŖĖŲ£¬Ō×ÓŠņŹżŅĄ“ĪŌö“ó£®AŌŖĖŲµÄµ„ÖŹŹĒæÕĘųµÄÖ÷ŅŖ³É·Ö£¬BŌ×ÓŗĖĶāp¹ģµĄÉĻÓŠ1¶Ō³É¶Ōµē×Ó£¬DŌŖĖŲµÄ¼Ūµē×ÓŹżŹĒĘäÓąµē×ÓŹżµÄŅ»°ė£¬CÓėBĶ¬Ö÷×壬AÓėFĶ¬Ö÷×壬DÓėEĶ¬×壮»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
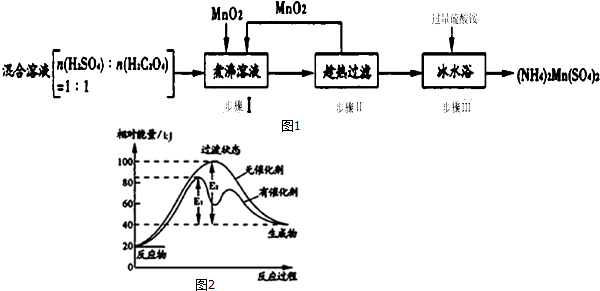
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
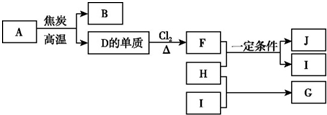 »ÆŗĻĪļAŹĒÖĘ²£Į§µÄÖ÷ŅŖŌĮĻÖ®Ņ»£®³£ĪĀĻĀ£¬»ÆŗĻĪļB”¢H”¢IĪŖĘųĢ壬B²»ČÜÓŚĖ®£¬H”¢IŅ×ČÜÓŚĖ®£¬HµÄĖ®ČÜŅŗ³Ź¼īŠŌ£¬IµÄĖ®ČÜŅŗ³ŹĖįŠŌ£®DŌŖĖŲŹĒµŲæĒÖŠŗ¬Įæ½ö“ĪÓŚŃõµÄ·Ē½šŹōŌŖĖŲ£®»ÆŗĻĪļJŹĒŅ»ÖÖæÉÓĆÓŚÖĘŌģ·¢¶Æ»śµÄŠĀŠĶĪŽ»ś·Ē½šŹō²ÄĮĻ£¬ĘäĻą¶Ō·Ö×ÓÖŹĮæĪŖ140£¬ĘäÖŠDŌŖĖŲµÄÖŹĮæ·ÖŹżĪŖ60%£®ÉĻŹöĪļÖŹ¼äµÄ×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾£®
»ÆŗĻĪļAŹĒÖĘ²£Į§µÄÖ÷ŅŖŌĮĻÖ®Ņ»£®³£ĪĀĻĀ£¬»ÆŗĻĪļB”¢H”¢IĪŖĘųĢ壬B²»ČÜÓŚĖ®£¬H”¢IŅ×ČÜÓŚĖ®£¬HµÄĖ®ČÜŅŗ³Ź¼īŠŌ£¬IµÄĖ®ČÜŅŗ³ŹĖįŠŌ£®DŌŖĖŲŹĒµŲæĒÖŠŗ¬Įæ½ö“ĪÓŚŃõµÄ·Ē½šŹōŌŖĖŲ£®»ÆŗĻĪļJŹĒŅ»ÖÖæÉÓĆÓŚÖĘŌģ·¢¶Æ»śµÄŠĀŠĶĪŽ»ś·Ē½šŹō²ÄĮĻ£¬ĘäĻą¶Ō·Ö×ÓÖŹĮæĪŖ140£¬ĘäÖŠDŌŖĖŲµÄÖŹĮæ·ÖŹżĪŖ60%£®ÉĻŹöĪļÖŹ¼äµÄ×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾£®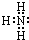 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | “ęŌŚµēĄėÖ»ÓŠHCO3-?H++CO32-£¬H2O?H++OH- | |
| B£® | HCO3-µÄµēĄė³Ģ¶Č“óÓŚHCO3-µÄĖ®½ā³Ģ¶Č | |
| C£® | c £ØNa+£©+c £ØH+£©ØTc £ØHCO3-£©+c £ØCO32-£©+c £ØOH-£© | |
| D£® | c £ØNa+£©ØTc £ØHCO3-£©+c £ØCO32-£©+c £ØH2CO3£© |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com