
| A.氧化还原反应的本质是元素化合价的升价 |
| B.氧化还原反应一定有氧元素参加 |
| C.氧化反应一定先于还原反应 |
| D.发生氧化反应的物质也可能同时发生还原反应 |
科目:高中化学 来源:不详 题型:单选题
| A.除①以外 | B.除③以外 | C.①②③⑤ | D.全部可以 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 CO2↑+Mn2++□。下列有关叙述正确的是 ( )
CO2↑+Mn2++□。下列有关叙述正确的是 ( )| A.发生还原反应的是C2O |
| B.该离子方程式右侧方框内的产物是OH- |
| C.8 mol H+参加反应时,电子转移5 mol |
| D.草酸分子只中只含有极性共价键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.9∶4 | B.5∶1 | C.11∶2 | D.1∶1 ( ) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 3Fe+4CO2的反应中, 是氧化剂, 是还原剂, 元素被氧化, 元素被还原。
3Fe+4CO2的反应中, 是氧化剂, 是还原剂, 元素被氧化, 元素被还原。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
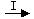 Fe3O4 ,Fe2O3
Fe3O4 ,Fe2O3 Fe 可知,欲实现I反应过程应从___________ (填“甲”或“乙”,下同)中找物质,欲实现II反应过程应从 中找物质。
Fe 可知,欲实现I反应过程应从___________ (填“甲”或“乙”,下同)中找物质,欲实现II反应过程应从 中找物质。 下面对应的横线上,组成一个配平了的化学方程式,并标出电子转移的方向和数目。(提示:反应物是Fe2O3和3 CO )
下面对应的横线上,组成一个配平了的化学方程式,并标出电子转移的方向和数目。(提示:反应物是Fe2O3和3 CO )


 + ="==== " +
+ ="==== " +  4NO+6H2O,则根据质量守恒定律可以推出X的化学式为 。
4NO+6H2O,则根据质量守恒定律可以推出X的化学式为 。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com