
 ijѧ���õ�����ȡ����ͭ���壬���о�����ͭ�ܷ�����������ȷֽ�ʵ����������ã�ʵ�鲽�����£�
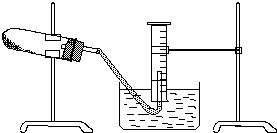
ijѧ���õ�����ȡ����ͭ���壬���о�����ͭ�ܷ�����������ȷֽ�ʵ����������ã�ʵ�鲽�����£����� 1��������������ձ��У���ˮ�Ƴ���Һʱ��Ҫ�ò��������裬���ٵ��������ܽ��ٶȣ�������ʱ�ò��������裬��Ϊ�˷�ֹ�ֲ��¶ȹ���ʹҺ�ηɽ�������ʱ�õ�������������������������ͭ�����һ������������ع��壬��Ͼ���Ҳ��Ҫ�������Ľ��裻
��2��ag�����к�ͭԪ������Ϊag��$\frac{64}{250}$=$\frac{32}{125}$a�������Ƶ�����ͭ������ΪX������ͭ�غ���X��$\frac{64}{80}$=$\frac{32}{125}$a�����X=$\frac{8}{25}$a���ݴ˼����ɵ����Ʊ�����ͭ�IJ��ʣ�
��3������pH��ֽ��ʹ�÷������⣻
��4��������Ҫ֤����Ӧǰ������ͭ���������䣬��Ӧ���Ƚ�����ͭ�ӻ�����з����������ˮ�ܽ⣬���й��ˣ��õ�������ͭ�����Ȼ�����Һ������ϴ�Ӹ���ٽ��г������ɣ�
��5��ͨ���Ա�ʵ�����˵������ͭ��ȷ�ӿ�������صķ�Ӧ�ٶȣ���ȡ��ͬ����������ع��壬��������ֱͭ�Ӽ��ȣ��Աȷų����������ʿ�������������ԣ�
��� �⣺��1��������������ձ��У���ˮ�Ƴ���Һʱ��Ҫ�ò��������裬���ٵ��������ܽ��ٶȣ�������ʱ�ò��������裬��Ϊ�˷�ֹ�ֲ��¶ȹ���ʹҺ�ηɽ�������ʱ�õ�������������������������ͭ�����һ������������ع��壬��Ͼ���Ҳ��Ҫ�������Ľ��裬����ѡ��٢ڢۢܣ�
�ʴ�Ϊ���٢ڢۢܣ�
��2��ag�����к�ͭԪ������Ϊag��$\frac{64}{250}$=$\frac{32}{125}$a�������Ƶ�����ͭ������ΪX������ͭ�غ���X��$\frac{64}{80}$=$\frac{32}{125}$a�����X=$\frac{8}{25}$a�������ɵ����Ʊ�����ͭ�IJ��ʣ�$\frac{b}{\frac{8}{25}a}$��100%=$\frac{25b}{8a}$��100%��
�ʴ�Ϊ��$\frac{25b}{8a}$��
��3���ⶨ��ҺpH�IJ���Ϊ����һС��pH��ֽ���ڱ�������Ƭ���ϣ���պ�л����Һ�IJ�����������ֽ���в�����ֽ��ɫ����ֽ��ɫ�������ɫ���Ƚ���ȷ����Һ��pH��
�ʴ�Ϊ����һС��pH��ֽ���ڱ�������Ƭ���ϣ���պ�л����Һ�IJ�����������ֽ���в�����ֽ��ɫ����ֽ��ɫ�������ɫ���Ƚ���ȷ����Һ��pH��
��4��������Ҫ֤����Ӧǰ������ͭ���������䣬��Ӧ���Ƚ�����ͭ�ӻ�����з����������ˮ�ܽ⣬���й��ˣ��õ�������ͭ�����Ȼ�����Һ������ϴ�Ӹ���ٽ��г�����
�ʴ�Ϊ��cadbe��
��5��ͨ���Ա�ʵ�����˵������ͭ��ȷ�ӿ�������صķ�Ӧ�ٶȣ���ȡ��ͬ����������ع��壬��������ֱͭ�Ӽ��ȣ��Աȷų����������ʿ�������������ԣ�
�ʴ�Ϊ���Ա�ʵ�飬��ȡ�������������أ����ȣ��Ƚϲ�����ͬ������������ʱ�䣬��Ƚ�����ͬʱ���ڲ��������������
���� ������Ҫ�������ʵ��Ʊ����ѶȲ����漰���ʼ��㡢ʵ��ԭ��������ʵ�����������ʵ�鷽������Ƶȣ�ע�����֪ʶ�����պ�������ã�


 Сѧ��ĩ���Ծ�ϵ�д�
Сѧ��ĩ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO32-��Cl- | B�� | Na+��Cu2+ | C�� | Mg2+��C1- | D�� | C1-��Ba2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 H2O2+
H2O2+ 6H+=
6H+= Mn2++
Mn2++ O2��+
O2��+ 8H2O��
8H2O��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
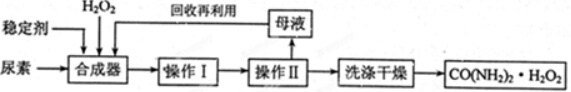
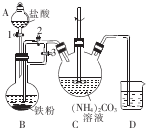 ��������{[CH3CH��OH��COO]2Fe}�㷺Ӧ��������Ʒ��Ӫ��Һ�ȣ�����ˮ������������FeCO3��Ӧ�Ƶã�
��������{[CH3CH��OH��COO]2Fe}�㷺Ӧ��������Ʒ��Ӫ��Һ�ȣ�����ˮ������������FeCO3��Ӧ�Ƶã��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
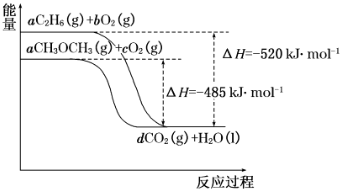
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��Ԫ�ؼȱ������ֱ���ԭ | |
| B�� | �������뻹ԭ�������ʵ���֮��Ϊ1��2 | |
| C�� | ÿ����1molNa2S2O3��ת��4mol���� | |
| D�� | ��ת��8mol����ʱ����ԭ��������������1mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
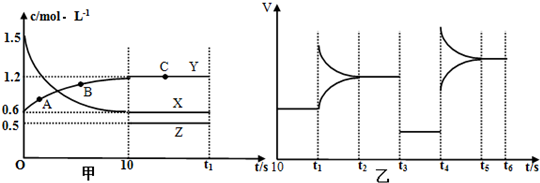
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 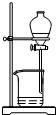 �ų���ı���Һ �ų���ı���Һ | B�� | 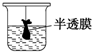 ������ᴿ���� ������ᴿ���� | ||
| C�� | 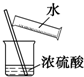 ʵ����ϡ��Ũ���� ʵ����ϡ��Ũ���� | D�� | 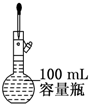 ���� ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com