
���� ��1�������ԣ���Ӧ�������ᱵ�������ƺ�ˮ���������1��2��Ӧ��
��2������ϡ���ᷴӦ������������NO�����ˮ��
��3����ҵ����ʯӢ����Ҫ�ɷ�ΪSiO2���Ʊ��ֹ裬�÷�ӦΪ���������ӷ�Ӧ��
��4���ö��Ե缫��ⱥ��ʳ��ˮʱ�����������ӷŵ��������������������ӵõ����������������÷�ӦΪ���ӷ�Ӧ��
��5������������̼�ʹ�����Ʒ�Ӧ����̼��Ƴ����ʹ����ᣬ�÷�ӦΪ���ӷ�Ӧ��
��6��ǿ����Һ��NaClO��Fe��OH��3��Ӧ����Na2FeO4���÷�ӦΪ���ӷ�Ӧ��
��� �⣺��1�������ԣ���Ӧ�������ᱵ�������ƺ�ˮ���������1��2��Ӧ����Ӧ�����ӷ�ӦΪ��2H++SO42-+Ba2++2OH-�T2H2O+BaSO4����
�ʴ�Ϊ��2H++SO42-+Ba2++2OH-�T2H2O+BaSO4����
��2������ϡ���ᷴӦ�����ӷ���ʽΪ��3Ag+4H++NO3-�T3Ag++NO��+2H2O�����Կ���ϡ����ϴ��������
�ʴ�Ϊ��3Ag+4H++NO3-�T3Ag++NO��+2H2O��
��3����ҵ����ʯӢ����Ҫ�ɷ�ΪSiO2���Ʊ��ֹ裬��Ӧ�Ļ�ѧ����ʽΪ��SiO2+2C$\frac{\underline{\;����\;}}{\;}$Si+2CO����
�ʴ�Ϊ��SiO2+2C$\frac{\underline{\;����\;}}{\;}$Si+2CO����
��4����ⱥ��ʳ��ˮ����Һ�е�������������ʧ���������������������������õ���������������������������������Ũ�����������������ƣ���Ӧ�����ӷ���ʽ��2Cl-+2H2O$\frac{\underline{\;���\;}}{\;}$2OH-+H2��+Cl2�����ʴ�Ϊ��2Cl-+2H2O$\frac{\underline{\;���\;}}{\;}$2OH-+H2��+Cl2����
��5��Ư����Һ��ͨ�������Ķ�����̼��������̼��ƺʹ����ᣬ��Ӧ�����ӷ���ʽΪCa2++2ClO-+H2O+CO2�TCaCO3��+2HClO��
�ʴ�Ϊ��Ca2++2ClO-+H2O+CO2�TCaCO3��+2HClO��
��6��ǿ����Һ��NaClO��Fe��OH��3��Ӧ����Na2FeO4���Ȼ��ƺ�ˮ����Ӧ�����ӷ�ӦΪ��2Fe��OH��3+3ClO-+4OH-�T2FeO42-+3Cl-+5H2O��
�ʴ�Ϊ��2Fe��OH��3+3ClO-+4OH-�T2FeO42-+3Cl-+5H2O��
���� ���⿼�����ӷ�Ӧ����ʽ����д��Ϊ��Ƶ���㣬���շ����ķ�Ӧ�����ӷ�Ӧ����д����Ϊ���Ĺؼ�������ˮ�ⷴӦ��������ԭ��Ӧ�����ӷ�Ӧ���飬ע�����ӷ�Ӧ�б�����ѧʽ�����ʼ����ӡ�����غ㣬�ۺ��Խ�ǿ����Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ƹ������ʹ�ù�����ͨ���߳��� | |
| B�� | �ոѾ͵ط��գ���������ɱ� | |
| C�� | ������չ̫���ܺͷ������� | |
| D�� | ��ȼú����������SO2�Կ�������Ⱦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
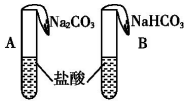 ijѧ����A��B����װ�õ������зֱ�װ��1.06g Na2CO3��0.84g NaHCO3���Թ����������ĵ�Ũ�ȡ�����������ᣬ��������������ͬʱ�����Թ�����ȫ��Ӧ���й�������������ȷ���ǣ����跴Ӧǰ����Һ������䣩��������
ijѧ����A��B����װ�õ������зֱ�װ��1.06g Na2CO3��0.84g NaHCO3���Թ����������ĵ�Ũ�ȡ�����������ᣬ��������������ͬʱ�����Թ�����ȫ��Ӧ���й�������������ȷ���ǣ����跴Ӧǰ����Һ������䣩��������| A�� | ���A��������ٶȿ죬����B����� | |
| B�� | ���B��������ٶȿ죬����������һ���� | |
| C�� | ��������Һ�����������ʵ���Ũ����ͬ | |
| D�� | ��������Һ�����������ʵ���Ũ�Ȳ�ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Һ��ֲ㣬�²�Ϊ���㣬��ɫ | B�� | Һ��ֲ㣬�²�Ϊˮ�㣬��ɫ | ||
| C�� | Һ��ֲ㣬�ϲ�Ϊ���㣬��ɫ | D�� | Һ��ֲ㣬�ϲ�Ϊˮ�㣬��ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������Ƶĵ���ʽ��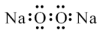 | B�� | ������Ľṹʽ��H-Cl-O | ||
| C�� | NH4Cl�ĵ���ʽ��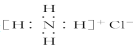 | D�� | ��ԭ�ӵĽṹʾ��ͼ��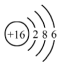 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ѹǿ���ٱ仯 | |
| B�� | C������������A���������ʵ�2�� | |
| C�� | ��λʱ��������amolA��ͬʱ����2amolC | |
| D�� | B������������ٱ仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 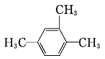 1��3��4-���ױ� 1��3��4-���ױ� | B�� | 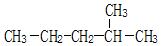 2-������ 2-������ | ||
| C�� | 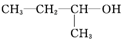 2-��-1-���� 2-��-1-���� | D�� | 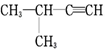 2-��-3-��Ȳ 2-��-3-��Ȳ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | c��N2��2 mol/L | B�� | c��N2��0 mol/L | C�� | c��H2��1 mol/L | D�� | c��NH3��2.5 mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
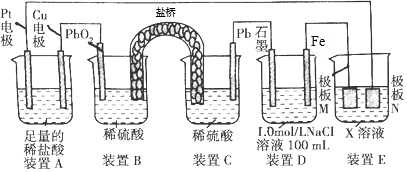
| A�� | װ��B��PbO2�Ϸ����ĵ缫��Ӧ����ʽΪ��PbO2+4H++SO42-+2e-�TPbSO4+2H2O | |
| B�� | װ��A���ܷ�Ӧ�����ӷ���ʽΪ��Cu+2H+$\frac{\underline{\;ͨ��\;}}{\;}$Cu2++H2�� | |
| C�� | ��װ��E��Ŀ������Cu�����϶�������N�IJ���ΪCu | |
| D�� | ����װ��D������0.2molFe��OH��3��������ˮ�����ʵ�����Ϊ0.5mol |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com