
ij����������л���������李�Ϊ�ⶨ�õ��ʵĺ�������һ��ѧ�о���ѧϰС����Ƶ�ʵ��װ��ͼ���¡���ش�������⣺
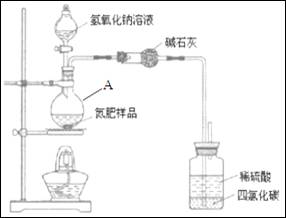
��1������A������Ϊ ��������м�ʯ�ҵ������� �����ƿ�����Ȼ�̼�������� ��
��2��д������������������������Һ��Ӧ�����ӷ���ʽ ��
��3��ָ����ʦָ�����ø�װ�ý���ʵ�飬��ʹ��������������ʵ��������ް������ݣ���õ���Ʒ�������Խ�ƫ�ͣ���ԭ������� ��
 ��ѧʵ����ϵ�д�
��ѧʵ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ñ���KOH��Һ�� ��δ֪Ũ�ȵ����ᣬ���ⶨ���ƫ�ͣ���ԭ�������(����)
��δ֪Ũ�ȵ����ᣬ���ⶨ���ƫ�ͣ���ԭ�������(����)
A�����Ʊ���Һ�Ĺ���KOH�л���NaOH����
B���ζ��յ����ʱ�����ӵζ��ܵĿ̶ȣ�����������ȷ
C��ʢװδ֪Һ����ƿ������ˮϴ��������δ֪Һ��ϴ
D���ζ����յ����ʱ�����ֵζ��ܼ��촦����һ����Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
Fe(OH)3�����MgCl2��Һ��ͬ���е�������
A������ɢϵ���ж������������ B�����Ƚ��ȶ����ܷ���ò���������
C�����������Ȳ�������������ܽ⡡��������  D����ɢ������ͨ����Ĥ
D����ɢ������ͨ����Ĥ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���е��뷽��ʽ�������
A��CaCl2 ��Ca2++2Cl�� B��Ba(OH)2��Ba2++2OH��
C��HNO3��H++NO3�� D��NaHCO3��Na++H++CO32��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ʵ������ȡ�����ķ�ӦΪ2KMnO4 == K2MnO4+MnO2 + 3O2 ������Ӧ���ʣ�����л��ն������̵IJ���˳����ȷ����
A���ܽ⡢���ˡ�ϴ�ӡ����� B���ܽ⡢���ˡ�������ϴ��
C���ܽ⡢������ϴ�ӡ����� D���ܽ⡢ϴ�ӡ����ˡ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�±�Ϊ�йػ������pKsp��pKsp����lgKsp��ijͬѧ���ʵ�����£�����AgNO3��Һ�м�������NaX��Һ���õ�����AgX��������м�NaY�������ת��ΪAgY��������м���Na2Z��������ת��ΪAg2Z�������a��b��c�Ĵ�С��ϵΪ(����)
| ��ػ����� | AgX | AgY | Ag2Z |
| pKsp | a | b | c |
A.a��b��c���������������� B��a��b��c
C��c��a��b D��a��b��c
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪Ksp(AgCl)=1.56��10-10��Ksp(AgBr)=7.7��10-13��Ksp(Ag2CrO4)=9.0��10-12��ij��Һ�к���Cl-��Br-��CrO ��Ũ�Ⱦ�Ϊ0.010mol •L-1�������Һ����μ���0.010 mol •L-1��AgNO3��Һʱ�����������Ӳ����������Ⱥ�˳��Ϊ ( )
��Ũ�Ⱦ�Ϊ0.010mol •L-1�������Һ����μ���0.010 mol •L-1��AgNO3��Һʱ�����������Ӳ����������Ⱥ�˳��Ϊ ( )
A��Cl-��Br-��CrO B��CrO
B��CrO ��Br-��Cl-
��Br-��Cl-
C��Br-��Cl-��CrO D��Br-��CrO
D��Br-��CrO ��Cl-
��Cl-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������Һ������Ũ�ȹ�ϵ����ȷ���� (����)
A��c(NH )>c(SO
)>c(SO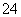 )>c(H��)>c(OH��)
)>c(H��)>c(OH��)
B��c(NH )��2c(SO
)��2c(SO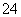 )
)
C��c(NH )��c(NH3·H2O)��2c(SO
)��c(NH3·H2O)��2c(SO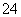 )
)
D��c(NH )��c(H��)��c(OH��)��2c(SO
)��c(H��)��c(OH��)��2c(SO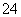 )
)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
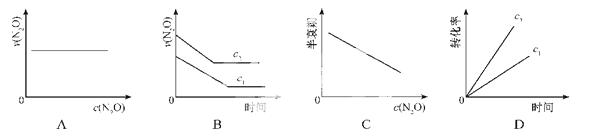
��һ�������£�N2O�ֽ�IJ���ʵ���������£�
| ��Ӧʱ��/min | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| c(N2O)/mol/L | 0.1 | 0.090 | 0.080 | 0.070 | 0.060 | 0.050 | 0.040 | 0.030 | 0.020 | 0.010 | 0.000 |
��ͼ����ȷ��ʾ�÷�Ӧ�й��������仯���ɵ���
(ע��ͼ�а�˥��ָ��һŨ��N2O����һ��ʱ�������Ӧʱ�䣬c1��c2����ʾN2O��ʼŨ����c1��c2)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com