
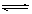 CH3OH(g) ������ΪCu2O/ZnO������������������и��⣺
CH3OH(g) ������ΪCu2O/ZnO������������������и��⣺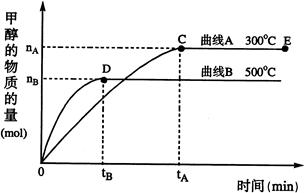



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 x C(g)���ڲ�ͬ�¶ȼ�ѹǿ��p1�� p2�������£���Ӧ��A��ת������ͼ��ʾ�������ж���ȷ����
x C(g)���ڲ�ͬ�¶ȼ�ѹǿ��p1�� p2�������£���Ӧ��A��ת������ͼ��ʾ�������ж���ȷ���� 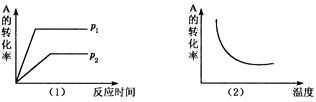
| A����H > 0�� m + n > x | B����H > 0�� m + n < x |
| C����H < 0�� m + n < x | D����H < 0�� m + n > x |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����ű���ʳ��ˮ���ռ�Cl2 | B���غ�ɫNO2��ѹ����ɫ�ȱ�����dz�� |
| C������ˮƿʱ���д������������ | D��H2��I2��HIƽ��������ѹ����ɫ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
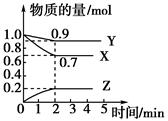
 CH3OH(g)
CH3OH(g) | A������CH3OH������������CO��������� |
| B�����������ܶȲ��� |
| C�������������ƽ�������������� |
| D��CH3OH��CO��H2��Ũ�ȶ����ٷ����仯 |
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
| CO | H2 | CH3OH |
| 0.5 mol��L-1 | 2mol��L-1 | 6mol��L-1 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 C(g)+D(g)�Ѵ�ƽ�����
C(g)+D(g)�Ѵ�ƽ����� | A��A���������ٷ����ı� | B������������ʵ������ٷ����ı� |
| C��C�ķ��������ٷ����ı� | D��D�����ʵ���Ũ�Ȳ��ٷ����ı� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 N2O4(g) �ﵽƽ��ʱ������������ͨ��һ������NO2��g�������´ﵽƽ������һ��ƽ��ʱ��ȣ�NO2����������� ��
N2O4(g) �ﵽƽ��ʱ������������ͨ��һ������NO2��g�������´ﵽƽ������һ��ƽ��ʱ��ȣ�NO2����������� ��| A������ | B������ | C����С | D�����ж� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 CO(NH2)2(l) �� H2O (l) ��H < 0 ���ش��������⣺
CO(NH2)2(l) �� H2O (l) ��H < 0 ���ش��������⣺ NH2COONH4(s) ��H1< 0
NH2COONH4(s) ��H1< 0 CO(NH2)2(l)�� H2O (l) ��H 2> 0
CO(NH2)2(l)�� H2O (l) ��H 2> 0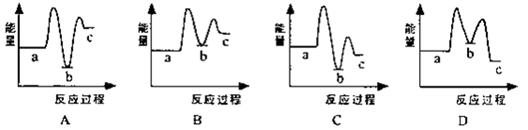
| A����С��Ӧ�������ݻ� |
| B�������¶� |
| C��ƽ����ϵ�м�ʱ�����CO��NH2��2 |
| D��ʹ�ú��ʵĴ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2HI(g) ��C(s)��H2O(g)
2HI(g) ��C(s)��H2O(g) CO(g)��H2(g)������״̬�ܱ�������Ӧ���ﵽƽ��״̬���ǣ� ��
CO(g)��H2(g)������״̬�ܱ�������Ӧ���ﵽƽ��״̬���ǣ� ��| A��abc | B��ade | C��ac | D��ae |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com