
A、Na+、Fe2+、Cl-、SO
| ||||||
B、K+、Na+、[Al(OH)4]-、NO
| ||||||
C、Ba2+、Na+、NO
| ||||||
D、NH
|
 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案科目:高中化学 来源: 题型:
| A、阴极析出7.04g铜 |
| B、阴极电极反应为:Cu2++2e-═Cu;2H++2e-═H2↑ |
| C、阳极电极反应为:4OH--4e-═2H2O+O2↑ |
| D、向电解后的溶液中加入铜最多溶解7.04g铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol氨基(-NH2)中含电子数为10NA |
| B、标况下,22.4 L N2和NO的混合气体所含的原子数为2NA |
| C、假设1 mol氯化铁完全转化为氢氧化铁胶体,则分散系中胶体微粒数为NA |
| D、在反应CaO+3C=CaC2+CO中,生成1 mol CO,转移的电子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、物质的量浓度相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液中c(NH4+):c(NH4)2SO4>c(NH4HSO4)>c(NH4C1) |
| B、向醋酸钠溶液中加入适量醋酸,得到酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| C、pH=6的纯水:c(H+)>c(OH-) |
| D、1.0mol/LNa2CO3溶液:c(OH-)=c(H+)+c(H2CO3)+c(HCO3-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mo1?L-1MgCl2溶液中含Cl-数为0.2 NA |
| B、1 L 0.1m01?L-1AlCl3溶液中,Al3+数为0.1NA |
| C、标准状况下,22.4L的CCl4中含CCl4分子数为NA |
| D、1mol铁与足量的Cl2反应,转移的电子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cl-、Mg2+、H+、Cu2+、SO42- |
| B、Na+、Ba2+、NO3-、OH-、SO42- |
| C、MnO4-、K+、Cl-、H+、SO42- |
| D、K+、NO3-、SO42-、OH-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
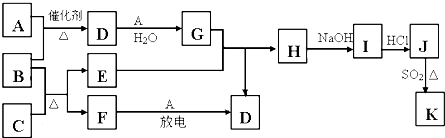
 A~H是中学化学常见的物质,它们之间的转化关系如图所示(部分产物已略去).已知B、D是生活中常见的金属单质,G是气体单质,C的焰色反应呈黄色.
A~H是中学化学常见的物质,它们之间的转化关系如图所示(部分产物已略去).已知B、D是生活中常见的金属单质,G是气体单质,C的焰色反应呈黄色.查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验操作 | 实验现象 | 实验结论或总结 | ||
| 各步骤结论 | 总结 | |||
| 实验一 | 将氯酸钾加热至融化,伸入带火星的木条, | 木条复燃 | 氯酸钾受热要分解产生氧气,但是 反应的化学方程式为: |
二氧化锰是氯酸钾受热分解的催化剂 |
| 实验二 | 将氯酸钾加热至融化,伸入带火星的木条, | 木条不复燃 | 二氧化锰受热不产生氧气 | |
| 实验三 | 木条迅速复 燃 | 二氧化锰能加快氯酸钾的分解 | ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com