
| A、电解饱和食盐水的阳极反应:2H2O+2e-=H2↑+2OH- | ||
B、碳酸钠溶液呈碱性的原因:CO
| ||
C、向AgNO3溶液中加入过量氨水:Ag++NH3?H2O=AgOH↓+NH
| ||
D、泡沫灭火器反应原理:A12++3HCO
|


 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:
 四川盛产五倍子.以五倍子为原料可以制得化合物A.A的结构简式如图所示:请回答下列问题:
四川盛产五倍子.以五倍子为原料可以制得化合物A.A的结构简式如图所示:请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将铜屑加入Fe3+溶液中:2Fe3++Cu=2Fe2++Cu2+ |
| B、向氢氧化钠溶液中通入少量CO2:CO2+OH-=HCO3- |
| C、铝片放入NaOH溶液中:2OH-+Al=AlO2-+H2↑ |
| D、往碳酸钙中滴加稀盐酸:CO32-+2H+=CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、12.5g |
| B、13.2g |
| C、19.7g |
| D、24.4g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 150℃ |
| 催化剂 |
| A、平衡时,其他条件不变,升高温度可使该反应的速率加快,平衡常数增大 |
| B、平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小 |
| C、平衡时,其他条件不变,增大压强,废气中氮氧化物的转化率减小 |
| D、平衡时,其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Br-.S2-.CO32-.K+ |
| B、Na+.NH4+.Cu2+.NO3- |
| C、Na+.K+.I-.Al3+ |
| D、Ba2+.Fe3+.Cl-.AlO2- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.2mol?L-1的NaHCO3溶液:c(HCO3-)>c(CO32-)>0.1mol?L-1>c(H2CO3) |
| B、pH=2的HCl溶液与pH=12的氨水等体积混合:c(Cl-)>c(NH+4)>c(H+)>c(OH-) |
| C、0.2mol?L-1CH3COOH溶液和0.2mol?L-1CH3COONa溶液等体积混合:c(CH3COO-)+c(OH-)-c(H+)=0.1mol?L-1 |
| D、0.1mol?L-1Na2CO3溶液与0.1mol?L-1NaHCO3溶液等体积混合:c(CO32-)+2c(OH-)=c(HCO-3)+3c(H2CO3)+2c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 用酒精萃取溴水中的溴 |
B、 将硫酸铜溶液直接蒸干得到胆矾 |
C、 说明2NO2(g)?N2O4(g)△H<0 |
D、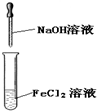 实验室制备Fe(OH)2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com