
容积均为1L的甲、乙两个恒容容器中,分别充入2molA、2molB和1molA、1molB,相同条件下,发生下列反应:A(g)+B(g) xC(g) △H<0。测得两容器中c(A)随时间t的变化如图所示,下列说法不正确的是
xC(g) △H<0。测得两容器中c(A)随时间t的变化如图所示,下列说法不正确的是
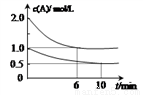
A. x=1
B. 此条件下,该反应的平衡常数K=4
C. 给乙容器升温可缩短反应达平衡的时间但不能提高平衡转化率
D. 甲和乙中B的平衡转化率相等
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源:2017届黑龙江省牡丹江市高三2月开学检测理综化学试卷(解析版) 题型:选择题
常温下,向20 mL 0.01 mol/L CH3COOH溶液中逐滴加入0.01 mol/L 的NaOH溶液,溶液中水所电离出的c(H+)随加入NaOH溶液的体积变化示意图如下,下列说法正确的是
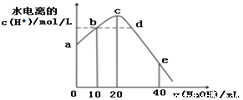
A. 从a到c,对醋酸的电离既有促进作用也有抑制作用
B. b、d两点溶液的pH相同
C. e点所示溶液中,c(Na+)=2c(CH3COO-)+2c(CH3COOH) = 0.01mol/L
D. 从b→d的过程中,既存在pH=7的点也存在水电离的c(H+)=10-7的点
查看答案和解析>>
科目:高中化学 来源:2017届湖南省衡阳市高三下学期第一次联考理综化学试卷(解析版) 题型:实验题
氯化亚铜(CuCl)在有机合成工业中常作催化剂。它是一种白色固体,微溶于水,易被空气中的氧气氧化。某研究性学习小组先在HCl气流中微热分解CuCl2·2H2O制无水CuCl2,再加热制备CuCl,并用下图所示装置进行相关实验探究(夹持仪器略)。
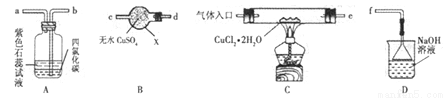
请回答下列问题:
(1)仪器X的名称是_________,装置连接顺序是 接_____、_____接_____、_____接f。
(2)实验操作的先后顺序是①→_____→_____→_____→⑤(填操作的编号)。
①检查装置的气密性后加入药品 ②熄灭酒精灯,冷却 ③在“气体入口”处通入干燥HCl
④点燃酒精灯,加热 ⑤停止通入HCl,然后通入N2其中通入N2气体的目的是________。
(3)在实验过程中,观察到B中物质由白色变为蓝色,A中上层溶液的颜色变化是______,下层CCl4的作用是①吸收少量Cl2;②________。
(4)装置D中发生的氧化还原反应的离子方程式为________。
(5)反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuO杂质,则产生的原因___________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省邯郸市高二下学期开学考试化学试卷(解析版) 题型:选择题
K、Ka、KW分别表示化学平衡常数、电离常数和水的离子积常数,下列判断正确的是
A. 在500℃、20 MPa条件下,在5 L密闭容器中进行合成氨的反应,使用催化剂后K增大
B. 室温下K(HCN)<K(CH3COOH),说明CH3COOH的电离度一定比HCN的大
C. 25℃时,pH均为4的盐酸和NH4I溶液中KW不相等
D. 2SO2+O2==2SO3达平衡后,改变某一条件时K不变,SO2的转化率可能增大、减小或不变
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省邯郸市高二下学期开学考试化学试卷(解析版) 题型:选择题
利用如图装置,完成很多电化学实验。下列有关此装置的叙述中,正确的是
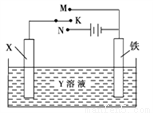
A. 若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阴极保护法
B. 若X为碳棒,Y为NaCl溶液,开关K置于N处,可减缓铁的腐蚀,溶液中的阴离子向铁电极移动
C. 若X为铜棒,Y为硫酸铜溶液,开关K置于M处,铜棒质量将增加,此时外电路中的电子向铜电极移动
D. 若X为铜棒,Y为硫酸铜溶液,开关K置于N处,铁棒质量将增加,溶液中铜离子浓度将减小
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省邯郸市高二下学期开学考试化学试卷(解析版) 题型:选择题
下列操作正确的是
A. 用pH试纸测得某新制氯水的pH值为3.5
B. 用酸式滴定管量取酸性高锰酸钾溶液5.10mL
C. 用标准盐酸溶液滴定一定体积的待测NaOH溶液时,用待测溶液润洗锥形瓶
D. 用l0 mL的量简量取8.05mL浓硫酸
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省六安市高一上学期期末考试化学试卷(解析版) 题型:填空题
(1)向某NaOH溶液中投入一块Al箔,先无明显现象,随后逐渐产生气泡,则产生气泡的离子反应方程式为______。
(2)实验室常用还原性Fe粉与水蒸气反应的实验来研究Fe的还原性,则该反应的化学反应方程式为______
(3)Fe(OH)2制备时,采用的方法是“长滴管、液面下”的实验操作,但在实验时,由于操作不当,依旧会出现白色沉淀、灰绿色沉淀直至最终变为红褐色沉淀,写出白色沉淀最终转化为红褐色沉淀的化学反应方程式为______
(4)实验时制备Al(OH)3时,常用可溶性铝盐(如Al2(SO4)3与氨水反应进行制备。某课外小组在实验时不慎向Al2(SO4)3溶液中加入了过量NaOH溶液,最终并没有制出白色沉淀Al(OH)3,则该小组同学实验时发生的总离子反应方程式为____。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省六安市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列表述不正确的是( )
A. 人造刚玉熔点很高,可用作高级耐火材料,主要成分是Al2O3
B. 硅是制造太阳能电池的常用材料
C. 四氧敏化三铁俗称铁红.可用作油漆、红色涂料
D. 分散系中分散质粒子的直径:Fe(OH)3恳浊液> Fe(OH)3胶体>FeCl3溶液
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省嘉峪关市高一上学期期末考试化学试卷(解析版) 题型:选择题
金属钠长期置于空气中,最后变为: ( )
A. Na2O B. Na2O2 C. NaOH D. Na2CO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com