
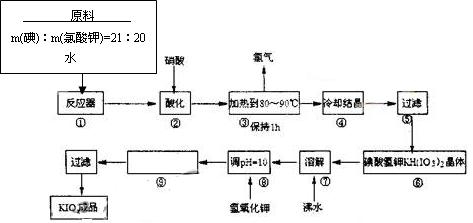
| 温度 | 0 | 10 | 20 | 40 | 60 | 80 |
| KIO3g/100g水 | 4.60 | 6.27 | 8.08 | 12.6 | 18.3 | 24.8 |


科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2ZnO+2SO2 2C+O2
2ZnO+2SO2 2C+O2 2CO ZnO+CO
2CO ZnO+CO Zn(g)+CO2
Zn(g)+CO2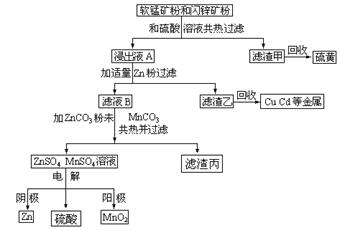
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
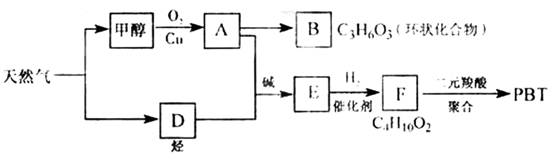
| A.取代反应 | B.加成反应 | C.酯化反应 | D.水解反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:判断题
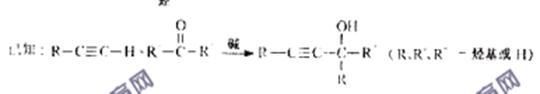
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.通过提高烟囱的高度可减少污染气体的排放 |
| B.电解Al2O3过程中加入冰晶石(Na3AlF6),可降低Al2O3熔融温度 |
| C.接触法制硫酸工业中,常常采用加压来提高SO2的转化率 |
| D.氯碱工业中,电解池两电极材料必须都要用耐腐蚀导电材料 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
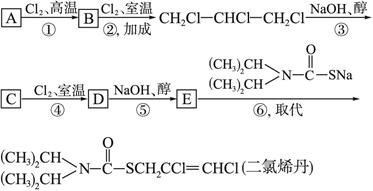
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用活性炭去除冰箱中的异味 |
| B.用热碱水清除炊具上残留的油污 |
| C.用浸泡过高锰酸钾溶液的硅藻土保存水果 |
| D.用含硅胶、铁粉的透气小袋与食品一起密封包装 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com