
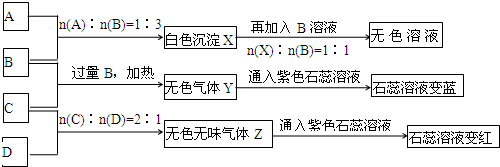
 HCO3-+OH-;HCO3-+H2O?H2CO3+OH-,故答案为:CO32-+H2O
HCO3-+OH-;HCO3-+H2O?H2CO3+OH-,故答案为:CO32-+H2O  HCO3-+OH-;HCO3-+H2O?H2CO3+OH-;
HCO3-+OH-;HCO3-+H2O?H2CO3+OH-;
| ||
| ||


 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 时间 | 开始 | 8h后 | 16h后 | 24h后 | 32h后 | 40h后 | 48h后 |
| pH | 5.0 | 4.8 | 4.6 | 4.3 | 4.2 | 4.0 | 4.0 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
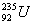 以后的副产品,其主要成分为低水平放射性的
以后的副产品,其主要成分为低水平放射性的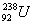 。下列有关
。下列有关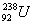 的说法正确的是( )
的说法正确的是( )| A.中子数为146 | B.质子数为238 |
| C.质量数为330 | D.核外电子数为146 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A | | | | | | | | | | | | | | | | | He |
| | | | | | | | | | | | | | | C | D | | |
| | E | | | | | | | | | | | F | | | | H | |
| | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | |
| | | | | | | | | | | | | | | | | | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com