
【题目】如图是元素周期表的一部分,请回答下列问题:
IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 | |
1 | ① | |||||||
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)在这些元素中,单质的化学性质最不活泼的是______________(填元素符号)。
(2)③的气态氢化物的电子式______________,②④形成的可溶于水的气态化合物的结构式______________。
(3)这些元素形成的最高价氧化物的水化物中,碱性最强的化合物为______________(填物质的化学式),酸性最强的含氧酸为______________(填物质的化学式)。
【答案】Ar ![]() O=C=O NaOH
O=C=O NaOH ![]()
【解析】
根据所给元素周期表,①为H元素,②为C元素,③为N元素,④为O元素,⑤为Na元素,⑥为Mg元素,⑦为S元素,⑧为Cl元素,⑨为Ar元素,据此分析。
(1)在这9种元素中,Ar为稀有气体元素,其化学性质最不活泼;
(2)③的气态氢化物为NH3,其电子式为![]() ;②④形成的可溶于水的气态化合物为CO2,其结构式为O=C=O;
;②④形成的可溶于水的气态化合物为CO2,其结构式为O=C=O;
(3)同周期从左到右元素的金属性逐渐减弱、非金属性逐渐增强,最高价氧化物对应水化物的碱性减弱、酸性增强;同主族从上到下元素的金属性逐渐增强、非金属性逐渐减弱,最高价氧化物对应水化物的碱性增强、酸性减弱;这些元素中Na的金属性最强,则其最高价氧化物对应的水化物NaOH的碱性最强,Cl的最高价氧化物对应的水化物HClO4的酸性最强。


科目:高中化学 来源: 题型:
【题目】元素周期表是学习化学的重要工具,它隐含着许多信息和规律。请根据下表中短周期元素的原子半径和主要化合价,回答表后问题。
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
原子半径(10-10 m) | 0.74 | 1.60 | 0.53 | 1.10 | 0.99 | 1.11 | 0.75 | 1.43 |
最高或最低化合价 | +2 | +1 | +5 | +7 | +2 | +5 | +3 | |
-2 | -3 | -1 | -3 |
(1)元素①在周期表中的位置为_____。
(2)元素①、⑦的氢化物的稳定性由强到弱的顺序为____(填化学式)。
(3)元素①、③形成的18电子化合物的电子式为____,元素②、⑧的最高价氧化物对应的水化物中,碱性较强的是______(填化学式)。
(4)元素②、⑤形成化合物的电子式为_____。
(5)元素⑤的最高价氧化物对应的水化物的水溶液与元素⑧的最高价氧化物对应水化物反应的离子方程式为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用所学化学知识解答问题:
(1)微粒![]() 中的质子数是_____,中子数是_____,核外电子数是_____。
中的质子数是_____,中子数是_____,核外电子数是_____。
(2)写出氯离子的原子结构示意图__,写出氯化钠的电子式___,用电子式表示HCl的形成过程___。
(3)NH4NO3是___化合物(填“离子”或“共价”),NaOH所含化学键类型为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:SO32-+I2+H2O→SO42-+2I-+2H+。某溶液中可能含有Na+、NH4+、Fe2+、K+、I-、SO32-、SO42-,且所有离子物质的量浓度相等。现取该溶液进行实验,操作和现象如下。有关该溶液的判断正确的是( )
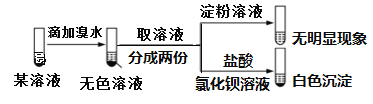
A.肯定不含I﹣B.可能不含SO42-
C.肯定含有SO32-D.肯定含有NH4+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高氯酸铵(![]() )是复合火箭推进剂的重要成分。通过如图所示的装置及实验步骤可以测定某高氯酸铵样品的纯度。
)是复合火箭推进剂的重要成分。通过如图所示的装置及实验步骤可以测定某高氯酸铵样品的纯度。
步骤1:检查装置气密性。
步骤2:准确称取样品![]() 于蒸馏烧瓶中,加入约
于蒸馏烧瓶中,加入约![]() 水溶解。
水溶解。
步骤3:准确量取![]() 溶液于锥形瓶中。
溶液于锥形瓶中。
步骤4:经仪器A向蒸馏瓶中加入![]() 溶液。
溶液。
步骤5:加热蒸馏至蒸馏烧瓶中剩余约100mL溶液。
步骤6:用新煮沸过的水冲洗冷凝装置2~3次,洗涤液并入锥形瓶中。
步骤7:向锥形瓶中加入酸碱指示剂,用![]() 标准溶液滴定至终点,消耗NaOH标准溶液
标准溶液滴定至终点,消耗NaOH标准溶液![]() 。
。
步骤8:将实验步骤1~7重复2次。

(1)仪器A的名称是______________。
(2)计算样品中高氯酸铵的质量分数_________(写出计算过程,已知杂质不参与反应)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关图像的说法正确的是

A. 图甲表示:向某明矾液中滴加过量的NaOH溶液,生成沉淀的物质的量与滴加NaOH溶液体积的关系
B. 图乙表示:向含等物质的量的NaOH和Na2CO3的混合溶液中滴加过量的稀盐酸,生成气体的体积与滴加HC1溶液体积的关系
C. 图丙表示:在稀硝酸溶液中加入过量的铁粉,溶液中Fe3+物质的量与加入铁粉物质的量的变化关系
D. 根据图丁,除去混在KNO3中少量的NaCl可用蒸发结晶的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是人类较早使用的金属之一。运用铁及其化合物的有关知识,回答下列问题:
(1)铁和铁合金是生活中的常用材料,下列叙述中,正确的是________。
A.纯铁硬度比生铁高
B.纯铁耐腐蚀性强,不易生锈
C.不锈钢是铁合金,只含金属元素
D.铁在一定条件下可与水蒸气反应
E.铁在冷的浓硫酸中钝化
(2)向沸水中逐滴加1mol/LFeCl3溶液,至液体呈透明的红褐色,该反应的离子方程式为____________,形成该分散系的微粒直径范围是_________。
(3)电子工业需用30%FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。请写出FeCl3溶液与铜反应的离子方程式_________。欲从腐蚀后的废液中回收铜并重新获得FeCl3溶液,现有下列试剂:①氯气、②铁粉、③浓硝酸、④浓盐酸、⑤烧碱、⑥浓氨水,需用用到的一组试剂是__________。
A. ①②④ B. ①③④⑥ C. ②④⑤ D. ①④⑥
(4)高铁酸钠Na2FeO3是一种新型净水剂。
①高铁酸钠主要通过如下反应制取:2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3X+5H2O,则X的化学式为__________。
②高铁酸钠在水中可以发生如下反应:FeO42-+10H2O=4Fe(OH)3+8OH-+3O2。由此看来,高铁酸钠能够杀菌消毒是因为它具有_____性,而能够除去水中悬浮物是因为________。
③下列物质能作净水削的有_________。
a.KAl(SO4)2·12H2O b.聚合硫酸铁[Fe(OH)(SO4)]n c.ClO2 d.“84消毒液”
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法正确的是
A. 18g重水(D2O)所含的电子数目为10NA
B. Na2O2与足量的水反应生成1 molO2,转移电子数目为2NA
C. 100 mL1 molL-1 FeCl3溶液中含有 Fe3+数目为 0.1NA
D. 将2molSO2和1molO2充分反应,转移的电子数目为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.H2(g)+I2(g) 2HI(g),其他条件不变,缩小反应容器体积,正逆反应速率不变
B.C(s)+H2O(g) H2(g)+CO(g),气体的总物质的量不再改变不能说明反应已达平衡
C.若压强不再随时间变化能说明反应2A(?)+B(g) 2C(?)已达平衡,则A、C不能同时是气体
D.1 mol N2和3 mol H2反应达到平衡时H2转化率为10%,放出的热量为Q1;在相同温度和压强下,当2 mol NH3分解为N2和H2的转化率为10%时,吸收的热量为Q2,Q2等于Q1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com