

| V��10-3L |
| 22.4L/mol |
| V��10-3L |
| 22.4L/mol |
| 56V |
| 22400 |
| 56V |
| 22400 |


 �Ƹ�С״Ԫͬ������������ϵ�д�
�Ƹ�С״Ԫͬ������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CH4?14H2O | ||
| B��CH4?8H2O | ||
C��CH4?7
| ||
| D��CH4?6H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
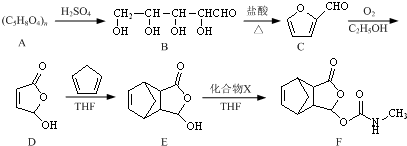
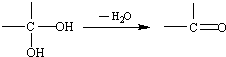
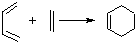
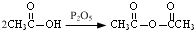
 ��
��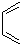 Ϊԭ�Ϻϳ�
Ϊԭ�Ϻϳ� ������ƺϳ�·�ߣ�ע����Ӧ��������
������ƺϳ�·�ߣ�ע����Ӧ��������| Ũ���� |
| 170�� |
| Br2 |
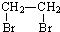
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


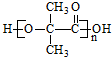 ���ĺϳ�·������ͼ�����Լ����ã����ϳ�·������ͼʾ�����£�
���ĺϳ�·������ͼ�����Լ����ã����ϳ�·������ͼʾ�����£�| Ũ���� |
| 170�� |
| Br2 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ˮ�ⷴӦ | ƽ�ⳣ����K�� |
| Fe3++3H2O?Fe��OH��3+3H+ | 7.9��10-4 |
| Fe2++2H2O?Fe��OH��2+2H+ | 3.2��10-10 |
| Cu2++2H2O?Cu��OH��2+2H+ | 3.2��10-7 |
| ʵ������ | ʵ������ |
| ��ͬѧ��ʵ�鷽�� | ��Һ�������ɫ��pH�������� |
| ��ͬѧ��ʵ�鷽�� | ����������pHû�����Ա仯�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ͭ���������������� |
| B������ͭ�������ڸ���Ļ����� |
| C������ͭ�������ڳ�ʪ�Ŀ����� |
| D������ͭ���ı��渲��һ������ĸ߷���Ĥ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������Һ������ֱ����10-9m��10-7m֮�䣬����ͨ��Һ������ֱ������10-7m |
| B��������Һ�����Ӳ�������Ĥ������ͨ��Һ������������Ĥ |
| C��������Һ�ж����ЧӦ������ͨ��Һ��û�� |
| D��������Һ���ȶ�������ͨ��Һ�ȶ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com