
【题目】下列有关实验装置、操作,不能实现相应实验目的的是
A | B | C | D | |
装置 |
|
|
|
|
目的 | 用KOH溶液除去溴苯中单质溴 | 证明浓硫酸有脱水性、强氧化性 | 先出现白色沉淀,后出现砖红色沉淀,证明Ksp(AgCl)< Ksp(Ag2CrO4) | 不能通过观察水能否全部流下来判断装置气密性 |
A. A B. B C. C D. D
【答案】C
【解析】
A.溴和NaOH反应生成可溶性的钠盐,溴苯不易溶于水,然后采用分液方法分离提纯溴苯,所以A选项是正确的;
B.浓硫酸具有脱水性和强氧化性,能将蔗糖脱水碳化(有黑色物质生成)并放出大量的热,在此条件下,碳可以把浓硫酸还原为二氧化硫,二氧化硫能使品红溶液褪色,故该过程可以证明浓硫酸表现了脱水性和强氧化性,所以B选项是正确的;
C. Ag2CrO4和AgCl的组成结构不相似,,不能依据先生成白色沉淀就判断氯化银的Ksp较小,只能依此判断氯化银的溶解度较小,故C错误;
D.该装置中分液漏斗和烧瓶通过橡皮管连接,可以使两者中的气压相同,打开分液漏斗的活塞后,分液漏斗中的水可以顺利完全流下,故不能依此判断该装置的气密性如何,故D选项是正确的。
故选C。


 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案科目:高中化学 来源: 题型:
【题目】实验室制备硝基苯(难溶于水,密度比水大的油状液体)的反应原理,下列关于硝基苯的制备和纯化的装置不正确的是
![]()
A. 浓硫酸与浓硝酸混合
B. 制备硝基苯
C. 用氢氧化钠溶液分离硝基苯中混有的酸
D. 分离硝基苯中混有的苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业以浓缩海水为原料提取溴的部分过程如下:
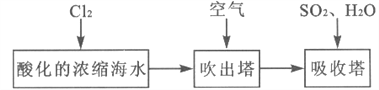
某课外小组在实验室模拟上述过程设计以下装置进行实验(所有橡胶制品均已被保护,夹持装置已略去):
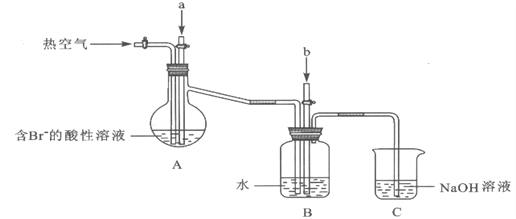
(1)实验开始时,A装置中不通热空气,先通入a气体的目的是(用离子方程式表示)_________。
(2)A装置中通入a气体一段时间后,停止通入,改通热空气。通入热空气的目的是_________。
(3)反应过程中,B装置中Br2与SO2反应的化学方程式____________________。
(4)C装置的作用是___________________。
(5)该小组同学向反应后B装置的溶液中通入氯气,充分反应得到混合液。
①一位同学根据溴的沸点是59℃,提出采用____________________方法从该混合液中分离出溴单质。
②另一位同学向该混合液中加入四氯化碳,充分振荡、静置后放出下层液体,这种方法是________。
(6)某同学提出证明反应后B装置的溶液中含有溴离子的实验方案是:取出少量溶液,先加入过量新制氯水,再加入KI淀粉溶液,观察溶液是否变蓝色。该方案是否合理并简述理由: _______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高锰酸钾是一种重要的化工原料,其绿色化制备是重要的课题。某课外小组设计如下方案用锰酸钾制备高锰酸钾。
I. 锰酸钾制备。将二氧化锰、氯酸钾和氢氧化钾固体放入铁坩埚熔融制锰酸钾。
(1)搅拌时用___________(填“铁棒”或“玻璃棒”)。
(2)若要制得锰酸钾59.1g,至少需要氯酸钾___________g。
II. 高锰酸钾制备。制备高锰酸钾的装置如下图所示(加热与夹持装置省略)。
用I制得的锰酸钾加少量蒸馏水溶解,得墨绿色溶液,倒入三颈瓶中。打开甲装置分液漏斗活塞加入稀硫酸,加热,生成乙酸蒸气,通入乙装置,水浴加热,搅拌,锰酸钾在酸性条件反应生成高锰酸钾和二氧化锰。
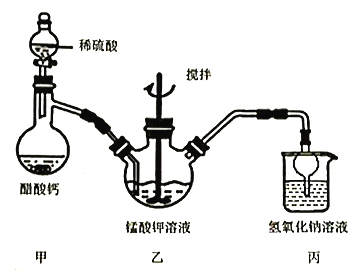
(3)用离子方程式表示甲装置中存在的化学平衡___________(任写一个)。
(4)乙装置中发生反应的化学方程式:______________________。
(5)丙装置中氢氧化钠溶液的作用是______________________。
(6)甲装置容易发生倒吸,改进的措施是______________________。
(7)判断乙装置中锰酸钾完全反应的实验方法是;用玻璃棒蘸取溶液滴到滤纸上,若观察到______________________, 表示锰酸钾已完全反应。
III.高锰酸钾产品的纯度分析。
(8)将乙中所得溶液过滤,把滤液倒入蒸发皿中,浓缩,冷却,抽滤,洗涤,干燥得KMnO4产品。请设计实验证明产品中含有少量MnO2:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某元素的价类二维图,其中A为正盐,X是一种强碱,通常条件下Z是无色液体,E的相对分子质量比D大16,各物质的转化关系如图所示。下列说法错误的是

A. A作肥料时不适合与草木灰混合施用
B. 同主族元素的氢化物中B的沸点最低
C. C一般用排水法收集
D. D→E的反应可用于检验D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:pOH=-lgc(OH-),温度为T℃时,向20.00mL 0.01mol·L-1氨水中滴入0.10mol·L-1的盐酸(不考虑溶质挥发),溶液的pH和pOH与加入盐酸体积关系如图所示。下列说法正确的是

A. 曲线PJN表示溶液中pH的变化
B. 若M点水的电离程度与Q点相等,则Q点一定符合c(Cl-)>c(NH4+)+c(NH3·H2O)
C. M、P两点的数值之和a+b=14
D. pH与pOH交叉点J对应的V(盐酸)=20.00mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯硝酸锶[Sr(NO3)2]可用于制造信号灯、光学玻璃等。工业级硝酸锶含硝酸钙、硝酸钡等杂质,提纯流程如下:

已知:①“滤液1”的主要溶质是Ca(NO3)2;“滤渣1”的成分为Ba(NO3)2、Sr(NO3)2;“滤渣2”的主要成分为 BaCrO4(杂质不与硝酸反应)。②铬酸(H2CrO4)为弱酸。
(1)“酸浸”不能采用高温的原因是_________________________________。
(2)相对于水洗,用浓HNO3洗涤的优点是_________________________________。
(3)“滤液2”中过量的H2CrO4被N2H4还原为Cr3+,同时放出无污染的气体,写出反应的离子方程式_______________________________________________________。
(4)在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)![]() Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=1.0×10-32,当c(Cr3+)降至1.0×10-5mol/L,认为Cr3+已经完全沉淀。现将还原后溶液的pH值调至4,此时Cr3+是否沉淀完全?______________________(列式计算)。
Cr3+(aq)+3OH-(aq),常温下,Cr(OH)3的溶度积Ksp=1.0×10-32,当c(Cr3+)降至1.0×10-5mol/L,认为Cr3+已经完全沉淀。现将还原后溶液的pH值调至4,此时Cr3+是否沉淀完全?______________________(列式计算)。
(5)已知Cr(OH)3类似Al(OH)3,还原后溶液的pH不能大于8的原因是:___________。(结合离子方程式说明理由)。
(6)为了测定“滤渣2”中 BaCrO4的含量,进行以下实验:

①判断Ba2+完全沉淀的方法:____________________________________________。
②“滤渣2”中BaCO4的质量分数为______________________(用代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
①检测乙醇中是否含有水可加入少量的无水硫酸铜,若变蓝则说明含水
②除 去乙醇中微量的水可加入金属钠,使其完全反应
③加热蒸馏含水的乙醇可获得无水乙醇
④在含 少量水的乙醇中加入石灰,然后再加热蒸馏可以获得无水乙醇
A.①③B.②④C.①④D.③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com