
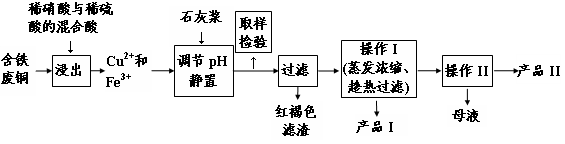
| �¶ȣ��棩 | 20 | 40 | 60 | 80 | 100 |
| ʯ�� | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| ���� | 32 | 44.6 | 61.8[ | 83.8 | 114 |
 2Fe2++I2����������Ϊ�������һ�����淴Ӧ��Fe3+��I����Ӧ�����Һ�����ɫ������I2����KI��Һ����ɫ��Ϊ̽�������ɫ��Һ���Ƿ�Fe3+������֤�����Ƿ���һ�����淴Ӧ��������ʵ���ҳ�����������Ʒ�������Լ���Ʒ�������дλ�ڴ�������±���0.1 mol/L��FeCl3��KI��KSCN��NaOH��H2SO4��KMnO4��Һ��CCl4������ˮ��
2Fe2++I2����������Ϊ�������һ�����淴Ӧ��Fe3+��I����Ӧ�����Һ�����ɫ������I2����KI��Һ����ɫ��Ϊ̽�������ɫ��Һ���Ƿ�Fe3+������֤�����Ƿ���һ�����淴Ӧ��������ʵ���ҳ�����������Ʒ�������Լ���Ʒ�������дλ�ڴ�������±���0.1 mol/L��FeCl3��KI��KSCN��NaOH��H2SO4��KMnO4��Һ��CCl4������ˮ��| ��� | ʵ����� | Ԥ������ͽ��� |
| �� | ���Թ��м�������FeCl3��Һ�� ������������������KI��Һ�� | ���ɫ���ڳ��� |
| �� | ���Թ��еĻ����Һת���� �����������У�����һ������ �� �� | |
| �� | | |
| ��� | ʵ����� | Ԥ������ͽ��� |
| �� | ������2�֣� | |
| �� | ��Һ©����1�֣���CCl4��1�֣�����ס�������������ȡ�������ã�1�֣� | Һ��ֲ㣬�ϲ�ӽ���ɫ���²��Ϻ�ɫ��1�֣� |
| �� | �������ȷų��²�Һ�壬�ٴӷ�Һ©�����Ͽ��е���ˮ�����Թ��У�����KSCN��Һ��2�֣� | ����Ѫ��ɫ����Ӧ��Ļ�����к�Fe3+������֤�����ȷ��һ�����淴Ӧ����֮��Fe3+������֤������һ�����淴Ӧ��2�֣� |


 ͬ��������ϰϵ�д�
ͬ��������ϰϵ�д� �ο�ͨ�γ̱�˼ά����������ѵ��ϵ�д�
�ο�ͨ�γ̱�˼ά����������ѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
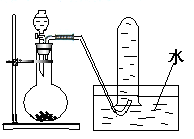
| A��Һ������㣬ʯ�����Ϊ��ɫ���л������ɫ |
| B��ʯ���Ϊ���㻷�����϶����������ϡ���ɫ |
| C��ʯ��������㣬�ϲ�Ϊ��ɫ���²�Ϊ��ɫ |
| D��ʯ���Ϊ���㻷�����϶����Ǻ졢�ϡ���ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Cl2 | B��SO2 | C��NO | D��NH3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Zn + 2HNO3(ϡ)= Zn(NO3)2 + H2�� |
B��CaCO3 + H2SO4(ϡ)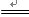 CaSO4 + H2O + CO2�� CaSO4 + H2O + CO2�� |
C��NH4Cl(aq) + NaOH(aq)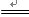 NaCl + H2O + NH3�� NaCl + H2O + NH3�� |
D��MnO2 + 4HCl(Ũ) 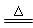 MnCl2 + Cl2��+ 2H2O MnCl2 + Cl2��+ 2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����������CaCO3��Ӧ��ȡCO2 | B����ϡ�����п��Ӧ��ȡH2 |
| C����NH4Cl��Ca(OH)2��Ӧ��ȡNH3 | D����H2O2��Һ��MnO2��Ӧ��ȡO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
| ���� | A | B | C |
| ��ʼŨ��/mol?L��1 | 0.020 | 0.020 | 0 |
| ƽ��Ũ��/mol?L��1 | 0.016 | 0.016 | 0.0080 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
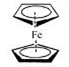
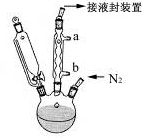
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
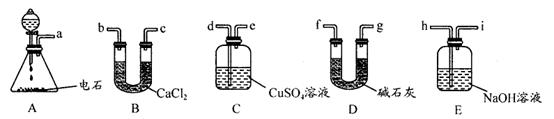

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��H2��CO2 | B��CO2��O2 | C��Cl2��NH3 | D��NH3��O2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com