
| A. | 向硝酸钙溶液里滴加稀盐酸得到pH=4的溶液中:2c(Ca2+)=c(NO3-) | |
| B. | 将0.2 mol•L-1NaA溶液和0.1 mol•L-1盐酸等体积混合所得的碱性溶液中(A-为酸根离子): c(Na+)>c(A-)>c(C1-)>c(OH-) | |
| C. | 0.1 mol/LNaAlO2溶液中:c(Na+)>c(AlO2-)>c(OH-)>c(H+) | |
| D. | 浓度均为0.1 mol•L-1的CH3COOH、CH3COONa的混合溶液中:2c(OH-)=2c(H+)+c(CH3COOH) |
分析 A.任何电解质溶液中都存在物料守恒,根据物料守恒判断;
B.二者混合后,溶液中的溶质为等物质的量浓度的NaA、NaCl、HA,混合溶液呈碱性,说明HA的电离程度小于A-水解程度;
C.NaAlO2是强碱弱酸盐,钠离子不水解,偏铝酸根离子水解导致溶液呈碱性,但水解程度较小;
D.任何电解质溶液中都存在电荷守恒和物料守恒,根据电荷守恒和物料守恒判断.
解答 解:A.任何电解质溶液中都存在物料守恒,硝酸根离子和钙离子都不水解,根据物料守恒得2c(Ca2+)=c(NO3-),故A正确;
B.二者混合后,溶液中的溶质为等物质的量浓度的NaA、NaCl、HA,混合溶液呈碱性,说明HA的电离程度小于A-水解程度,氯离子不水解,所以c(A-)<c(C1-),故B错误;
C.NaAlO2是强碱弱酸盐,钠离子不水解,偏铝酸根离子水解导致溶液呈碱性,但水解程度较小,所以c(OH-)>c(H+),结合电荷守恒得c(Na+)>c(AlO2-),所以离子浓度大小顺序是c(Na+)>c(AlO2-)>c(OH-)>c(H+),故C正确;
D.任何电解质溶液中都存在电荷守恒和物料守恒,根据电荷守恒得c(CH3COO-)+c(OH-)=c(H+)+c(Na+),根据物料守恒得2c(Na+)=c(CH3COO-)+c(CH3COOH),所以得c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH),故D错误;
故选AC.
点评 本题考查离子浓度大小比较,为高频考点,涉及盐类水解、弱电解质的电离,明确溶液中的溶质及溶液酸碱性是解本题关键,利用电荷守恒、物料守恒分析解答,易错选项是A,注意硝酸钙是强电解质,不水解,钙离子、硝酸钙离子浓度与溶液酸碱性无关.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 化学键包括共价键、离子键、金属键、氢键 | |
| B. | 单键都是σ键 | |
| C. | 化学键都有方向性和饱和性 | |
| D. | 极性共价键都是σ键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al2(SO4)3=2Al3++3SO42- | B. | HF=H++F- | ||
| C. | H3PO4?3H++PO43- | D. | NaHCO3=Na++H++CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 2NaHCO3═Na2CO3+CO2↑+H2O | B. | MnO2+4 HCl(浓)═MnCl2+Cl2↑+2 H2O | ||
| C. | 2 H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2 H2O+O2↑ | D. | Na2CO3+CaCl2═CaCO3↓+2NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
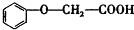 发生酯化反应的产物A是一种食用香料.甲分子为链状结构且不含甲基.回答下列问题:
发生酯化反应的产物A是一种食用香料.甲分子为链状结构且不含甲基.回答下列问题: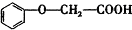 的分子式为C8H8O3.
的分子式为C8H8O3.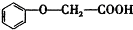 有多种同分异构体,其中属于酯类,能使FeCl3溶液显紫色,且苯环上的一氯代物有两种的同分异构体的结构简式为
有多种同分异构体,其中属于酯类,能使FeCl3溶液显紫色,且苯环上的一氯代物有两种的同分异构体的结构简式为 、
、 、
、 (其中一种)(任写一种).
(其中一种)(任写一种).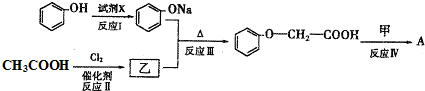
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分散系:盐酸、硫酸铜、空气 | B. | 电解质:烧碱、硫酸、盐酸 | ||
| C. | 盐:氯化钠、硫酸铝、碳酸钙 | D. | 非电解质:石墨、CO2、蔗糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com