
【题目】下图是中学常见物质间的转化关系。已知:
①A为淡黄色固体,B为导致“温室效应”的主要物质; ②E为常见金属,J为红褐色沉淀;
③G在实验室中常用于检验B的存在;④L是一种重要的工业原料,常用于制造炸药,浓溶液常呈黄色,储存在棕色瓶中。
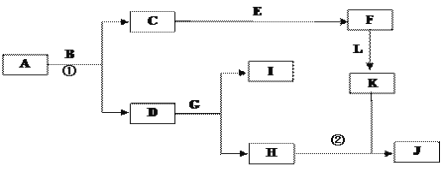
回答下列问题:
(1)A的电子式____________________________________________________。
(2)反应①的化学方程式为__________,反应②的离子方程式为_________________,
(3)若参加反应的A的质量为39g,则消耗CO2的体积(标况下)为__________L。
(4)L的化学式__________,G的化学式__________________________。
【答案】![]() 2Na2O2+2CO2=2Na2CO3+O2 Fe3++3OH-=Fe(OH)3↓ 11.2 HNO3 Ca(OH)2
2Na2O2+2CO2=2Na2CO3+O2 Fe3++3OH-=Fe(OH)3↓ 11.2 HNO3 Ca(OH)2
【解析】
A为淡黄色固体,B为导致“温室效应”的主要物质,二者发生反应,则A为Na2O2,B为CO2,二者反应生成Na2CO3和O2,G在实验室中常用于检验CO2的存在,则G为Ca(OH)2,故C为O2,D为Na2CO3,金属E经过系列反应得到J为红褐色沉淀,则J为Fe(OH)3,E为Fe,F为Fe3O4,L是一种重要的工业原料,常用于制造炸药,浓溶液若保存不当常呈黄色,应是浓硝酸所具有的性质,则L为HNO3,K为Fe(NO3)3,H为NaOH,I为CaCO3;据以上分析解答。
(1)由上述分析可以知道,A为Na2O2 ,电子式为![]() ;
;
因此,本题正确答案是:![]() ;
;
(2)反应①的化学方程式为: 2Na2O2+2CO2=2Na2CO3+O2;反应②的离子方程式为:Fe3++3OH-= Fe(OH)3↓;
因此,本题正确答案是: 2Na2O2+2CO2=2Na2CO3+O2;Fe3++3OH-= Fe(OH)3↓;
(3)n(Na2O2)=39÷78=0.5mol,由2Na2O2+2CO2=2Na2CO3+O2反应可知,则消耗CO2的体积(标况下)为0.5×22.4=11.2L;
因此,本题正确答案是: 11.2;
(4)结合以上分析可知,L的化学式HNO3,G的化学式为Ca(OH)2;
因此,本题正确答案是: HNO3;Ca(OH)2。


科目:高中化学 来源: 题型:
【题目】某同学进行如下实验![]() 溶液的浓度均为
溶液的浓度均为![]() 。
。
编号 | ① | ② | ③ |
实验 |
|
|
|
现象 | 产生无色气泡 | 产生无色气泡液面上方呈浅红棕色 | 产生无色气泡 |
下列对实验现象的解释或推测不合理的是
A.![]() 中:
中:![]()
B.根据上述实验判断,![]() 的氧化性强于水
的氧化性强于水
C.![]() 中:
中:![]()
D.![]() 中使湿润pH试纸变蓝的气体是
中使湿润pH试纸变蓝的气体是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某稀硫酸和稀硝酸的混合溶液![]() ,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解
,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解![]() 。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示
。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示![]() 已知硝酸只被还原为NO气体
已知硝酸只被还原为NO气体![]() 。下列分析或结果错误的是
。下列分析或结果错误的是

A.原混合酸中![]() 的物质的量为
的物质的量为![]()
B.OA段产生的是NO,AB段发生的反应为![]() ,BC段产生氢气
,BC段产生氢气
C.第二份溶液中最终溶质为![]()
D.![]() 浓度为
浓度为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[2012·南通二调](12分)碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂,在医药上也可用于治疗消化性溃疡出血。工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如下:
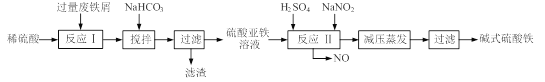 已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
开始沉淀 | 2.3 | 7.5 | 3.4 |
完全沉淀 | 3.2 | 9.7 | 4.4 |
回答下列问题:
(1)加入少量NaHCO3的目的是调节pH,使溶液中的 沉淀,该工艺中“搅拌”的作用是 。
(2)在实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,O2与NaNO2在反应中均作 。若参与反应的O2有11.2L(标准状况),则相当于节约NaNO2的物质的量为 。
(3)碱式硫酸铁溶于水后产生的Fe(OH)2+离子,可部分水解生成Fe2(OH)42+聚合离子。该水解反应的离子方程式为 。
(4)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁。根据我国质量标准,产品中不得含有Fe2+及NO3-。为检验所得产品中是否含有Fe2+,应使用的试剂为 。
A.氯水 B.KSCN溶液 C.NaOH溶液 D.酸性KMnO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设![]() 为阿伏加德罗常数的值( )
为阿伏加德罗常数的值( )
A.标准状况下,将![]() 通入水中发生反应,转移的电子数为
通入水中发生反应,转移的电子数为![]()
B.常温常压下, 7g乙烯和丁烯的混合物含有的极性键数目为![]()
C.将![]() 与过量
与过量![]() 反应转移的电子数为
反应转移的电子数为![]()
D.标准状况下,![]() 中所含电子数为
中所含电子数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,属于取代反应的是
①CH3CH=CH2+Br2![]() CH3CHBrCH2Br
CH3CHBrCH2Br
②CH3CH2OH![]() CH2=CH2+H2O
CH2=CH2+H2O
③CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
④C6H6+HNO3![]() C6H5NO2+H2O
C6H5NO2+H2O
A. ①②B. ③④C. ①③D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属氟化物一般都具有高容量、高质量密度的特点。氟离子热电池是新型电池中的一匹黑马,其结构如图所示。下列说法正确的是

A. 图示中与电子流向对应的氟离子移动方向是(B)
B. 电池放电过程中,若转移1mol电子,则M电极质量减小12g
C. 电池充电过程中阳极的电极反应式为:B+3F--3e-=BiF3
D. 该电池需要在高温条件下工作,目的是将热能转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1 g物质完全燃烧时的反应热叫做该物质的热值。有以下能量转化图,下列说法不正确的是( )
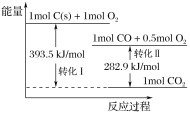
A.转化Ⅰ的热化学方程式为:C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
B.转化Ⅱ的热化学方程式为:2CO(g)+O2(g)=2CO2(g) ΔH=-565.8 kJ·mol-1
C.由C→CO的热化学方程式为:2C(s)+O2(g)=2CO(g) ΔH=-110.6 kJ·mol-1
D.CO的热值:ΔH=-10.1 kJ·g-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物(X)的结构简式如下图,下列关于它的说法不正确的是( )
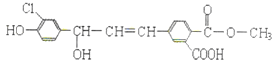
A.X遇FeCl3溶液能发生显色反应
B.一定条件下,X能发生取代、水解、氧化、加成、加聚等反应
C.1mol X分别与足量的NaOH、氢气反应,最多能消耗4mol NaOH 、7mol 氢气
D.等物质的量的该有机物分别与足量的Na、NaHCO3反应时,则消耗Na、NaHCO3的物质的量之比是3:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com