
某药物结构简式如图,该物质1mol与足量NaOH溶液反应,消耗的NaOH物质的量为( )
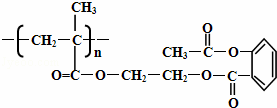
|
| A. | 3mol | B. | 4mol | C. | 3n mol | D. | 4n mol |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
下列各溶液中,Na+物质的量浓度最大的是( )
|
| A. | 2L 0.5mol/L NaCl溶液 | B. | 3L 0.3mol/L Na2SO4溶液 |
|
| C. | 1L 0.4mol/L Na2CO3溶液 | D. | 4L 0.15mol/L Na3PO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)请把符合要求的化学方程式的字母填在下列空白处:
①既属于分解反应又是氧化还原反应的是 .
②既属于化合反应,又是氧化还原反应的是 .
③不属于四种基本反应类型的氧化还原反应的是 .
A.(NH4)2SO3 2NH3↑+H2O+SO2↑ B.2CO+O2
2NH3↑+H2O+SO2↑ B.2CO+O2 CO2
CO2
C. 2C+SiO2 Si+2CO↑ D.NH4NO3
Si+2CO↑ D.NH4NO3 N2O+2H2O
N2O+2H2O
E.CaCO3+CO2+H2O=Ca(HCO3)2F.MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(2)在氧化还原化学反应中(2CuO+C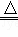 2Cu+CO2),物质所含元素化合价升高,这种物质是 剂,在反应中 (“得”或“失”)电子;元素化合价降低,表明该元素的原子在反应中 (“得”或“失”)电子.
2Cu+CO2),物质所含元素化合价升高,这种物质是 剂,在反应中 (“得”或“失”)电子;元素化合价降低,表明该元素的原子在反应中 (“得”或“失”)电子.
(3)鲜榨苹果汁是人们喜爱的饮料.由于此饮料中含有Fe2+,现榨的苹果汁在空气中会由淡绿色的Fe2+变为棕黄色Fe3+.这个变色的过程中的Fe2+被 (“氧化”或“还原”).若在榨汁的时候加入适量的维生素C,可有效防止这种现象的发生.这说明维生素C有 (“氧化”或“还原”)性.
查看答案和解析>>
科目:高中化学 来源: 题型:
具有单双键交替长链(如…一CH=CH﹣CH=CH﹣CH=CH一…)的高分子有可能成为导电塑料,2000年诺贝尔化学奖即授予开辟此领域的3位科学家.下列高分子中,可能成为导电塑料的是( )
|
| A. | 聚乙烯 | B. | 聚氯乙烯 | C. | 聚苯乙烯 | D. | 聚乙炔 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列所示的微粒中,氧化性最强的是( )
|
| A. | 1S22S22P2 | B. | 1S22S22P5 | C. | 1S22S22P63S1 | D. | 1S22S22P6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物A能与NaOH溶液反应,其分子中含有苯环,相对分子质量为136,其中含碳的质量分数为70.6%,氢的质量分数为5.9%,其余为氧.
(1)A的分子式是 .
(2)若A能与NaHCO3溶液反应放出CO2气体,其结构有种.
(3)若A与NaOH溶液在加热时才能反应,且1mol A消耗1mol NaOH,则A的结构简式可能是 .
(4)若A与NaOH溶液在加热时才能反应,且1mol A消耗2mol NaOH,则符合条件的A的结构可能有 4 种,其中能发生银镜反应的有 种,不能发生银镜反应的物质的结构简式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液可能含有Cl–、SO42–、CO32–、NH4+、Fe2+、Al3+和K+。取该溶液100 mL,加入过量NaOH溶液,加热,得到0. 02 mol气体,同时产生沉淀;过滤、洗涤、灼烧,得到1.6 g红棕色固体;向上述滤液中加入足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀。由此可知原溶液中( )
A.至少存在4种离子
B.Cl– 一定存在,且c(Cl )≥0.4 mol/L
C.SO42–、NH4+,一定存在,Cl–可能不存在
D.CO32–、Al3+ 一定不存在,K+可能存在
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学用语的使用正确的是
A.硫酸酸化的淀粉KI溶液在空气中变成蓝色:4I-+O2+2H2O==2I2+4OH-
 B.钢铁发生吸氧腐蚀时,正极的电极反应式:O2+4e-+2H2O==4OH-
B.钢铁发生吸氧腐蚀时,正极的电极反应式:O2+4e-+2H2O==4OH-
C.氨气催化氧化生产硝酸的主要反应: 4NH3+3O2 2N2↑+6H2O
D.向Na2SiO3溶液中通入过量CO2:SiO32-+2CO2+2H2O===H2SiO3+CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
图中X、Y、Z为单质,其他为化学物,它们之间存在如下转化关系(部分产物已略去)。其中,A俗称磁性氧化铁;E是不溶于水的酸性氧化物,能与氢氟酸反应。
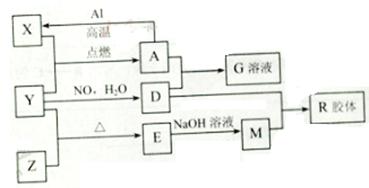
回答下列问题:
(1)组成单质Y的元素在周期表中的位置是 ;M中存在的化学键类型为 ;R的化学式是 。
(2)一定条件下,Z与H2反应生成ZH4,ZH4的电子式为 。
(3)已知A与1molAl反应转化为X时(所有物质均为固体)。放出aKJ热量。写出该反应的热化学方程式:
。
(4)写出A和D的稀溶液反应生成G的离子方程式:
(5)向含4mol D的稀溶液中,逐渐加入X粉末至过量。假设生成的气体只有一种,请在坐标系中画出n(X2+)随n(X)变化的示意图,并标出n(X2+)的最大值。
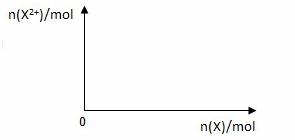
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com