
在一定条件下的密闭容器中,可逆反应A(g)+3B(g)2C(g)(g表示气态),在下列四种状态中处于平衡状态的是( )
| 速率 | A | B | C | D |
| v正/mol·(L·s)-1 | vA=1 | vB=2 | vA=1 | vC=1 |
| v逆/mol·(L·s)-1 | vB=1 | vC=2 | vC=2 | vC=2 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
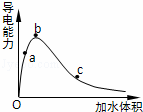
一定温度下,将一定质量的冰醋酸加水稀释,溶液的导电能力变化如图所示,下列说法中,正确的是( )
|
| A. | a、b、c三点溶液的pH:c<a<b |
|
| B. | a、b、c三点醋酸的电离程度:a<b<c |
|
| C. | 若用湿润的pH试纸测量a处溶液的pH,测量结果偏小 |
|
| D. | a、b、c三点溶液用1mol/L氢氧化钠溶液中和,消耗氢氧化钠溶液体积:c<a<b |
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物分子中基团间的相互影响会导致化学性质不同.下列叙述不能说明上述观点的是( )
|
| A. | 甲苯与硝酸作用可得到2,4,6﹣三硝基甲苯,而苯与硝酸作用得到硝基苯 |
|
| B. | 甲苯可以是高锰酸钾溶液退色,而甲烷不能 |
|
| C. | 乙烯可发生加成反应,而乙烷不能 |
|
| D. | 苯酚能与NaOH溶液反应,而乙醇不能 |
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上从废铅蓄电池的铅膏回收铅的过程中,可用碳酸盐溶液与处理后的铅膏(主要成分为PbSO4)发生反应:PbSO4(s)+CO32-(aq) PbCO3(s)+SO42-(aq)。某课题组用PbSO4为原料模拟该过程,探究上述反应的实验条件及固体产物的成分。
PbCO3(s)+SO42-(aq)。某课题组用PbSO4为原料模拟该过程,探究上述反应的实验条件及固体产物的成分。
(1)上述反应的平衡常数表达式:K=
(2)室温时,向两份相同的PbSO4样品中分别加入同体积、同浓度的Na2CO3和NaHCO3溶液均可实现上述转化。在 溶液中PbSO4转化率较大,理由是
(3)查阅文献:上述反应还可能生成碱式碳酸铅[2PbCO3·Pb(OH)2],它和PbCO3受热都易分解生成PbO。该课题组对固体产物(不考虑PbSO4)的成分提出如下假设。请你完成假设二和假设三:
假设一:全部为PbCO3;
假设二: ;
假设三: 。
(4)为验证假设一是否成立,课题组进行如下研究:
①定性研究:请你完成下表中内容
| 实验步骤(不要求写出具体操作过程) | 预期的实验现象和结论 |
| 取一定量样品充分干燥, |
②定量研究:取26.7 mg的干燥样品,加热,测
得固体质量随温度的变化关系如下图。某同学
由图中信息得出结论:假设一不成立。你是否
同意该同学的结论,并简述理由:
查看答案和解析>>
科目:高中化学 来源: 题型:
某工业废水中可能含有如下几种阴阳离子:
| 阳离子 | Fe3+、Al3+、Fe2+、Ba2+、Na+ |
| 阴离子 | Cl-、CO32-、NO3-、SO42-、SiO32- |
现对该废水样品进行以下研究:
Ⅰ.向试管中滴加浓盐酸,有少量的无色气体生成,气体遇空气立即变为红棕色;
Ⅱ.若向Ⅰ所得的溶液中加入BaCl2溶液,有白色沉淀生成。
Ⅲ.若向Ⅰ所得的溶液中加入过量的NaOH溶液,有红褐色沉淀生成。过滤后向所得滤液中通入过量的CO2气体,有白色絮状沉淀生成。
根据上述实验,回答下列问题:
(1)该废水中一定含有的阴离子是 ,一定不含有的阳离子是 ;
(2)写出Ⅲ的所得滤液中通入过量的CO2气体生成白色絮状沉淀的离子方程式(只写这一个): ;
(3)已知用铝粉可以除去废水中的一种阴离子(X)。若控制溶液的pH为10.7左右,再加入铝粉,除去X离子的同时产生氨气和氮气,且体积比为1﹕4,完成下列反应的离子方程式并配平:(X用具体的离子符号表示)
Al + X + OH- =AlO2-+ NH3 + N2 +
该反应的还原产物是 。若除去0.2mol X离子,要消耗铝 g。
(4)若将废水中的铁元素完全转化成Fe3+,此时测得c(Fe3+)=1.0×10-2mol·L-1,要想将其转换为Fe(OH)3沉淀而除去,则应调节溶液pH至少大于 。(已知常温下Fe(OH)3的Ksp=1.0×10-38)
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,可逆反应2AB+3C,在下列四种状态中,处于平衡状态是( )
正反应速率 逆反应速率
A.vA=2 mol·L-1·min-1 vB=2 mol·L-1·min-1
B.vA=2 mol·L-1·min-1 vC=2 mol·L-1·min-1
C.vA=1 mol·L-1·min-1 vB=2 mol·L-1·min-1
D.vA=1 mol·L-1·min-1 vC=1.5 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,在密闭容器中进行反应3SiCl4(g)+2N2(g)+6H2(g)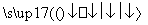 Si3N4(s)+12HCl(g),能表示上述反应达到化学平衡状态的是( )
Si3N4(s)+12HCl(g),能表示上述反应达到化学平衡状态的是( )
A.3v逆(N2)=v正(H2)
B.v正(HCl)=4v正(SiCl4)
C.混合气体密度保持不变
D.c(N2):c(H2):c(HCl)=1:3:6
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与社会、生活和生产息息相关,以下叙述错误的是( )
|
| A. | 科学家们正在研究利用蓝绿藻等低等植物和微生物在阳光作用下使水分解产生氢气 |
|
| B. | 贮氢金属在一定温度和压强下可以吸附氢气,如镧镍合金(LaNi5)可以吸附氢气形成LaNi5H6,其中H元素以化合态形式存在 |
|
| C. | 生活垃圾送入焚烧炉产生的热量可发电、供暖,焚烧炉产生的气体可直接排放 |
|
| D. | 2013年3月底,H7N9型禽流感在上海和安徽两地率先发现.要杀死禽流感病毒可通过消毒剂杀菌,通过加热煮沸杀菌,也可用紫外线照射杀菌 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某工厂排放的工业废水中可能含有K+、Ag+、NH4+、Mg2+、SO42﹣、Cl﹣、NO3﹣、HCO3﹣等离子.经检测废水呈明显的碱性,则可确定该厂废水中肯定不含有的离子组合是( )
|
| A. | Ag+、K+、NO3﹣、HCO3﹣ | B. | K+、NH4+、NO3﹣、SO42﹣ |
|
| C. | Ag+、NH4+、Mg2+、HCO3﹣ | D. | K+、Mg2+、SO42﹣、Cl﹣ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com