
判断正误,正确的划“√”,错误的划“×”
(1)强电解质溶液中不存在溶质分子,弱电解质溶液中存在溶质分子( )
(2)氨气溶于水,当c(OH-)=c(NH )时,表明NH3·H2O电离处于平衡状态( )
)时,表明NH3·H2O电离处于平衡状态( )
(3)弱电解质一定是共价化合物( )
(4)由0.1 mol·L-1一元碱BOH的pH=10,可知溶液中存在BOH===B++OH-( )
科目:高中化学 来源: 题型:
硫代硫酸钠溶液与稀硫酸反应的化学方程式为Na2S2O3+H2SO4===Na2SO4+SO2↑+S↓+H2O,下列各组实验中最先出现浑浊的是( )
| 选项 | 反应温度/℃ | Na2S2O3溶液 | 稀H2SO4 | H2O | ||
| V/mL | c/mol·L-1 | V/mL | c/mol·L-1 | V/mL | ||
| A | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
| B | 25 | 5 | 0.2 | 5 | 0.2 | 10 |
| C | 35 | 5 | 0.1 | 10 | 0.1 | 5 |
| D | 35 | 5 | 0.2 | 5 | 0.2 | 10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在容积为2 L的密闭容器中,有反应:mA(g)+nB(g)pC(g)+qD(g),经过5分钟达到平衡,此时各物质的变化为A减少a mol·L-1,B的平均反应速率v(B)=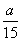 mol·L-1· min-1,C增加
mol·L-1· min-1,C增加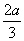 mol·L-1,这时若增加系统压强,发现A与C的百分含量不变,则m∶n∶p∶q为( )
mol·L-1,这时若增加系统压强,发现A与C的百分含量不变,则m∶n∶p∶q为( )
A.3∶1∶2∶2 B.1∶3∶2∶2
C.1∶3∶2∶1 D.1∶1∶1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,在2 L的恒容密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
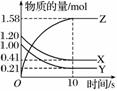
(1)从反应开始到10 s时,用Z表示的反应速率为__________,X的物质的量浓度减少了________,Y的转化率为______。
(2)该反应的化学方程式为______________________________________。
(3)10 s后的某一时刻(t1)改变了外界条件,其速率随时间的变化图像如图所示。则下列说法符合该图像的是______。
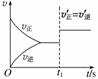
A.t1时刻,增大了X的浓度
B.t1时刻,升高了体系温度
C.t1时刻,缩小了容器体积
D.t1时刻,使用了催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
已知0.1 mol·L-1的醋酸溶液中存在电离平衡:CH3COOHCH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)的值增大,可以采取的措施是( )
①加少量烧碱溶液 ②升高温度 ③加少量冰醋酸 ④加水
A.①② B.①③ C.②④ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
按要求画出图像,并回答下列问题。
(1)相同体积、相同浓度的盐酸和醋酸
①加入足量的Zn,在甲图中画出H2体积的变化图像

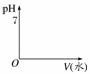
甲 乙
单位时间内,________产生的H2多,反应停止时,产生的H2________。
查看答案和解析>>
科目:高中化学 来源: 题型:
运用电离常数判断可以发生的反应是( )
| 酸 | 电离常数(25 ℃) |
| 碳酸 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
| 次溴酸 | Ki=2.4×10-9 |
①HBrO+Na2CO3===NaBrO+NaHCO3
②2HBrO+Na2CO3===2NaBrO+H2O+CO2↑
③HBrO+NaHCO3===NaBrO+H2O+CO2↑
④NaBrO+CO2+H2O===NaHCO3+HBrO
A.①③ B.②④
C.①④ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
根据实际和经验推知,下列叙述不正确的是( )
A.卤化氢易溶于水,不易溶于四氯化碳
B.碘易溶于汽油,微溶于水
C.氯化钠易溶于水,也易溶于食用油
D.丁烷易溶于煤油,难溶于水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com