

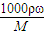 计算该浓硫酸的物质的量浓度,再根据稀释定律计算需要浓硫酸的体积;
计算该浓硫酸的物质的量浓度,再根据稀释定律计算需要浓硫酸的体积; mol/L=18.4mol/L,令需要该浓硫酸的体积为V,根据稀释定律,则:18.4mol/L×V=250mL×4.6mol/L,解得V=62.5mL,故C正确;
mol/L=18.4mol/L,令需要该浓硫酸的体积为V,根据稀释定律,则:18.4mol/L×V=250mL×4.6mol/L,解得V=62.5mL,故C正确;

科目:高中化学 来源: 题型:
 如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此回答下列问题:
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:单选题
 如图是某校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容,据此下列说法正确的是
如图是某校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容,据此下列说法正确的是查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com