
分析 (1)若固体恰好全部溶解,发生反应Fe2O3+3H2SO4=Fe2 (SO4)3+3H2O、Cu+Fe2 (SO4)3=2FeSO4+CuSO4,总反应方程式为Cu+Fe2O3+3H2SO4=CuSO4+2FeSO4+3H2O,
若Cu、Fe2O3按物质的量1:1混合,消耗的硫酸最少,若混合物粉末全是Fe2O3,消耗的硫酸最多,结合方程式计算解答;
(2)硫酸溶液过量,若铜过量,过量的铜不与硫酸反应,则只发生如下反应:Cu+Fe2O3+3H2SO4=CuSO4+2FeSO4+3H2O,根据溶液中n(Fe2+)计算n(Fe2O3),进而计算Cu的质量;
若Fe2O3过量,过量的Fe2O3将与H2SO4反应,根据溶液中n(Fe2+)计算Cu的质量.
解答 解:(1)若固体恰好全部溶解,铜粉和三氧化二铁的混合物是按如下反应进行:
Fe2O3+3H2SO4=Fe2 (SO4)3+3H2O、Cu+Fe2 (SO4)3=2FeSO4+CuSO4
总反应方程式为:Cu+Fe2O3+3H2SO4=CuSO4+2FeSO4+3H2O,
Cu、Fe2O3按物质的量1:1混合,消耗的硫酸最少,则n(Cu)=n(Fe2O3)=$\frac{22.4g}{64g/mol+160g/mol}$=0.1mol,由方程式可知,需要硫酸为0.1mol×3=0.3mol,硫酸体积为$\frac{0.3mol}{1mol/L}$=0.3L,
若混合物粉末全是Fe2O3,消耗的硫酸最多,则发生:Fe2O3+3H2SO4=Fe2 (SO4)3+3H2O,n(Fe2O3)=$\frac{22.4g}{160g/mol}$=0.14mol,故消耗H2SO4为0.14 mol×3=0.42 mol,硫酸体积为$\frac{0.42mol}{1mol/L}$=0.42L
但铜的质量不可能为0,故有0.3L≤V<0.42L,
答:范围为0.3L≤V<0.42L;
(2)溶液中n(Fe2+)=1L×0.1mol/L=0.1mol,则
Cu+Fe2O3+3H2SO4=CuSO4+2FeSO4+3H2O
0.05 0.05 0.1
若铜过量,过量的铜不与硫酸反应,则m (Fe2O3)=0.05 mol×160 g/mol=8.0 g,故m (Cu)=22.4 g-8.0 g=14.4 g;
若Fe2O3过量,过量的Fe2O3将与H2SO4反应,则m (Cu)=0.05mol×64 g/mol=3.2g,
答:含Cu为3.2或14.4
点评 本题考查混合物的有关计算,属于讨论型题目,利用总方程式简化分析与计算,注意(1)中利用极端法确定极值,(2)中不能确定铁离子与Cu是否恰好反应.


科目:高中化学 来源: 题型:实验题
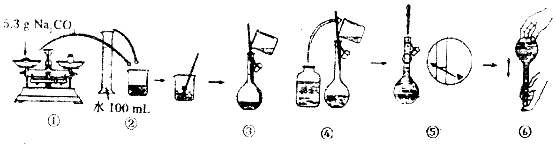
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  互为同分异构体 互为同分异构体 | |
| B. |  与 与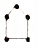 两种烃互为同系物 两种烃互为同系物 | |
| C. | 甲苯与溴蒸汽的反应产物受反应条件的影响而不同 | |
| D. | H2和D2互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{3a}{2}$ mol | B. | $\frac{a}{18}$ mol | C. | $\frac{a}{27}$ mol | D. | $\frac{a}{96}$ mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色溶液中:Na+、Cl-、SO42-、Cu2+ | |
| B. | 滴加紫色石蕊试液显红色的溶液:NH4+、Fe2+、SO42-、NO3- | |
| C. | 滴加酚酞显红色的溶液:K+、Ba2+、Cl-、NO32- | |
| D. | 含有大量HS-的溶液:NH4+、Ca2+、H+、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HOCH2CHO能发生取代反应、加成反应、氧化反应和还原反应 | |
| B. | 乙醇醛糖属于醛和糖的混合物 | |
| C. | HOCH2CHO与乙酸、甲酸甲酯互为同分异构体 | |
| D. | 乙醇醛糖与葡萄糖具有相似的化学性质 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
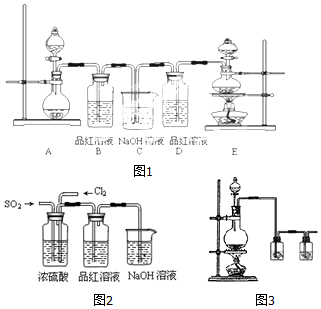
| 测试时间/h | 0 | 1 | 2 | 3 | 4 |
| 雨水的pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com