
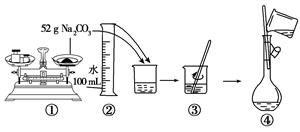
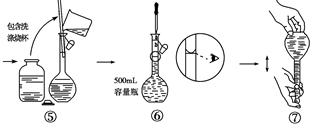


 �·Ƿ��̸����100��ϵ�д�
�·Ƿ��̸����100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��55% | B��60% | C��65% | D��70% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
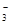 ��SO42-��Fe3+��H+��M�������ʵ���֮��Ϊ��n��NO
��SO42-��Fe3+��H+��M�������ʵ���֮��Ϊ��n��NO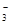 ���Un��SO42�����Un��Fe3+���Un��H
���Un��SO42�����Un��Fe3+���Un��H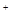 ���Un��M����2�U3�U1�U3�U1����M�����������е�
���Un��M����2�U3�U1�U3�U1����M�����������е�| A��Fe2+ | B��Cu2+ | C��Al3+ | D��Ba2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��0.2 mol | B��0.4 mol | C��0.6 mol | D��0.8 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��16��9 g����������BaO2����������������������ԼΪ0��2 NA |
| B�����³�ѹ�£�28 g��ϩ�ͻ����飨C4H8���Ļ�������к��е�̼ԭ����Ϊ2 NA |
C��a gij���庬������Ϊb��c g�������ڱ���µ����Ϊ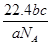 L L |
| D��ij�ܱ�����ʢ��0��1 molN2��0��3 molH2����һ�������³�ַ�Ӧ��ת�Ƶ��ӵ���ĿΪ0��6 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��NA��Fe��OH��3�������ӵ�����Ϊ107g |
| B��8��0 gCu2S��CuO�Ļ�����к���ͭԭ����Ϊ0��1NA |
| C����״���£�2��24 L Cl2����ˮ�дﵽ���ͣ��ɵõ�HClO���ӵ���Ŀ��0��1NA |
| D��2��3gNa��������ȫ��Ӧ����Ӧ��ת�Ƶĵ���������0��1 NA��0��2 NA֮�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����״����2.24 L H2O�У�������Ϊ0.1NA |
| B����1mol Cl2ͨ�뵽ˮ�У���N��HClO��+ N��Cl?��+ N��ClO-��= 2NA |
| C�����³�ѹ��16g O2��O3��������У���ԭ����ΪNA |
| D��7.8g Na2O2������ˮ��Ӧ��ת�Ƶ�����Ϊ0.2NA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com