
【题目】Ⅰ.用重铬酸钾法(一种氧化还原滴定法)可测定产物Fe3O4中的二价铁含量。若需配制浓度为0.01000 mol·L-1的K2Cr2O7标准溶液250 mL,应准确称取________ g K2Cr2O7(保留4位有效数字,已知M(K2Cr2O7)=294.0 g·mol-1)。
配制该标准溶液时,下列仪器中不必要用到的有________(用编号表示)。
①电子天平 ②烧杯 ③量筒 ④玻璃棒 ⑤容量瓶 ⑥胶头滴管 ⑦移液管
Ⅱ.四氯化硅粗产品经精馏后,得到的残留物中常含有铁元素,为了分析残留物中铁元素的含量,先将残留物预处理,使铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式是:5Fe2++MnO+8H+===5Fe3++Mn2++4H2O。
滴定前是否要滴加指示剂?________(填“是”或“否”),请说明理由__________________。
Ⅲ.某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.1000 mol/L Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。
①可选用______作滴定指示剂,滴定终点的现象是_______________________________。
②CuCl2溶液与KI反应的离子方程式为________________________________________。
③碘与硫代硫酸钠反应的离子方程式是________________________________________。
④该试样中CuCl2·2H2O的质量百分数为________。
【答案】 0.7350 ③⑦或⑦ 否 MnO有色,故不需其他指示剂 淀粉溶液 溶液的蓝色褪去,且30s内不恢复蓝色 2Cu2++4I- = 2CuI↓+I2 I2+2S2O32- = S4O62-+2I- 95%
【解析】Ⅰ.n(K2Cr2O7)=0.010 00 mol·L-1×0.25 L=0.002 5 mol,m(K2Cr2O7)=0.002 5 mol×294.0 g·mol-1=0.735 0 g;配制固体溶液时选用电子天平,配制液体时可选用量筒或移液管。故配制该标准溶液时,不必用到量筒、移液管。
Ⅱ.由于高锰酸钾本身是紫红色的,与Fe2+反应时,可以褪色,故而可以作为指示剂。
Ⅲ.①“间接碘量法”测定含有CuCl2·2H2O晶体试样的纯度的基本原理是CuCl2氧化I-生成I2,用Na2S2O3标准溶液滴定生成的I2,而淀粉溶液遇I2显蓝色,故可用淀粉溶液作指示剂,达到滴定终点时,溶液由蓝色变成无色,且半分钟内溶液不恢复原来的颜色。
②CuCl2与KI发生氧化还原反应,离子方程式为2Cu2++4I- = 2CuI↓+I2 。
③由题给信息可得关系式:2Cu2+~I2~2 Na2S2O3,则有
n(CuCl2·2H2O)=n(Cu2+)=n(Na2S2O3)=0.100 0 mol·L-1×20.00×10-3 L=2.000×10-3 mol,m(CuCl2·2H2O)=2.000×10-3 mol×171 g·mol-1=0.342 g。试样中CuCl2·2H2O的质量分数为![]() ×100%=95%。
×100%=95%。


科目:高中化学 来源: 题型:
【题目】(实验室制备1,2-二溴乙烷的反应原理是先用乙醇制备出乙烯,再将乙烯通入溴水中可制得1,2—二溴乙烷。已知制取乙烯的过程中还可能有少量乙醚、SO2等产物。现用少量的溴和足量的乙醇制备1,2—二溴乙烷的装置如图所示,有关数据列表如下。


请回答下列问题:
(1)写出装置A中制备乙烯的化学方程式______________________________________________。
(2)用两个化学方程式表示该实验中可能存在的副反应:_________________,_______________。
(3)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在________层(填“上”、“下”)。
(4)若产物中有少量副产物乙醚,可采用____________(填操作名称)的方法除去;若产物中有少量未反应的Br2,最好用_________洗涤除去(填正确选项前的字母)。
A.水 B.氢氧化钠溶液 C.碘化钠溶液 D.乙醇
(5)反应过程中应用冷水冷却装置 D,其主要目的是____________________________________。
(6)请设计实验方案证明1,2—二溴乙烷含有溴元素。(仪器和药品自选)________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家最近研究出一种环保、安全的储氢方法,其原理可表示为:储氢释氢NaHCO3+H2 ![]() HCOONa+H2O下列有关说法正确的是( )
HCOONa+H2O下列有关说法正确的是( )
A.储氢、释氢过程均无能量变化
B.NaHCO3、HCOONa均含有离子键和共价键
C.储氢过程中,NaHCO3被氧化
D.释氢过程中,每消耗0.1molH2O放出2.24L的H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如下图所示。则下列离子组在对应的溶液中,一定能大量共存的是( )
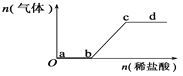
A. a点对应的溶液中:Na+、OH-、SO![]() 、NO
、NO![]()
B. b点对应的溶液中:Al3+、Fe3+、MnO![]() 、Cl-
、Cl-
C. c点对应的溶液中:Na+、Ca2+、NO![]() 、Cl-
、Cl-
D. d点对应的溶液中:F-、NO![]() 、Fe3+、Ag+
、Fe3+、Ag+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式错误的是( )
A. 向Ba(OH)2溶液中滴加稀硫酸:Ba2++2OH-+2H++SO![]() ===BaSO4↓+2H2O
===BaSO4↓+2H2O
B. 酸性介质中KMnO4氧化H2O2:2MnO![]() +5H2O2+6H+===2Mn2++5O2↑+8H2O
+5H2O2+6H+===2Mn2++5O2↑+8H2O
C. 等物质的量的MgCl2、Ba(OH)2和HCl溶液混合:Mg2++2OH-===Mg(OH)2↓
D. 铅酸蓄电池充电时的阳极反应:PbSO4+2H2O-2e-===PbO2+4H++SO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雷雨天闪电时空气中有臭氧生成,下列说法不正确的是 ( )
A. O2和O3互为同位素 B. O2和O3的相互转化是化学变化
C. 等物质的量的O2和O3含有的质子数不相同 D. 在相同的温度与压强下,等体积的O2和O3含有相同的分子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是一个制取氯气并以氯气为原料进行特定反应的装置,多余的氯气可以贮存在b瓶中,其中各试剂瓶中所装试剂为:B(氢硫酸)、C(碘化钾淀粉溶液)、D(水)、F(紫色石蕊试液). 
(1)若A中烧瓶中的固体为MnO2 , 液体为浓盐酸,则其发生反应的化学方程式为 .
(2)如何检查装置G的气密性:(写出操作方法和现象).
(3)G中b瓶内宜加入的液体是;实验开始后B中的现象是 , C中的现象是 , F的现象是 .
(4)E装置中硬质玻璃管内盛有炭粉,若E中发生氧化还原反应,其产物为二氧化碳和氯化氢,写出E中反应的化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用电子式表示下列物质的结构:
(1)NH4Cl;
(2)Na2O2;
(3)CO2;
(4)MgCl2;(1)~(6)中,仅含离子键的是 , 仅含共价键的是 , 既有离子键又有共价键的是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com