

 .
.分析 A俗称磁性氧化铁,即为Fe3O4;能与氢氟酸反应且不溶于水的酸性氧化物是SiO2,即E为SiO2,根据框图中的转化关系,可知X为Fe、Y为O2、Z为Si、D为硝酸、M为Na2SiO3、G为硝酸铁,R为H2SiO3,结合对应的物质的性质以及题目要求可解答该题.
解答 解:A俗称磁性氧化铁,即为Fe3O4;能与氢氟酸反应且不溶于水的酸性氧化物是SiO2,即E为SiO2,根据框图中的转化关系,可知X为Fe、Y为O2、Z为Si、D为硝酸、M为Na2SiO3、G为硝酸铁,R为H2SiO3,
(1)组成单质Y的元素为O元素,原子核外有2个电子层,最外层电子数为6,位于元素周期表中第二周期,第ⅥA族,M为Na2SiO3,存在的化学键类型为离子键和共价键,R为H2SiO3,
故答案为:第二周期第ⅥA族;离子键和共价键; H2SiO3;
(2)Z为Si,Z与H2反应转化为SiH4,SiH4的电子式为 ,故答案为:
,故答案为: ;
;
(3)Fe3O4在高温下可与铝发生铝热反应,方程式为8Al+3Fe3O4$\frac{\underline{\;高温\;}}{\;}$9Fe+4Al2O3,故答案为:8Al+3Fe3O4$\frac{\underline{\;高温\;}}{\;}$9Fe+4Al2O3;
(4)四氧化三铁和硝酸反应是氧化物中的二价铁元素被氧化到最高价,硝酸中氮元素被还原到+2价,反应的离子方程式为:3Fe3O4+28H++NO3-=9Fe3++NO↑+14H2O,
故答案为:3Fe3O4+28H++NO3-=9Fe3++NO↑+14H2O;
(5)铁和稀硝酸反应,开始铁全部被硝酸氧化为硝酸铁,故开始阶段Fe2+的量为0,随着铁的加入,多余的铁又和Fe3+反应而生成Fe2+,故Fe2+的量逐渐会增大直至到最大值,以后不变,反应过程中生成的气体为NO,令Fe2+的最大物质的量为xmol,根据电子转移守恒可知,NO的物质的量=$\frac{xmol×2}{3}$,根据N元素守恒可知:$\frac{xmol×2}{3}$+2x mol=4 mol,解得x=1.5,故n(Fe2+)随n(Fe)变化的示意图为: ,
,
故答案为: .
.
点评 本题考查无机物的推断,侧重物质转化和性质的考查,侧重铝热反应及硅及其化合物转化的考查,(5)为易错点,注意根据反应的方程式计算,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 由分子组成的物质中一定存在共价键 | |
| B. | 由非金属元素组成的化合物一定是共价化合物 | |
| C. | 非极性键只存在双原子分子中 | |
| D. | 两个非金属元素原子间不可能形成离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
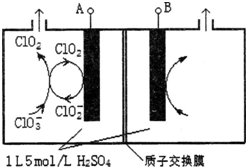 研究含Cl、N、S等元素的化合物对净化水质、防治污染有重要意义.
研究含Cl、N、S等元素的化合物对净化水质、防治污染有重要意义.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 化合物A、B可合成荧光“魔棒”中产生能量的物质之一(CPPO).
化合物A、B可合成荧光“魔棒”中产生能量的物质之一(CPPO).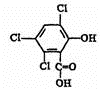 .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com