
(10分)计算填空:
(1)(2分)1mol某金属单质与足量的H2SO4反应,放出1.5molH2(标况下)并转化为具有Ne原子的电子层结构的离子,则该金属在周期表的位置 。
(2)(6 分)已知在2L的容器中进行下列可逆反应,各物质的有关数据如下:
_
aA (g)+ bB (g)  2C(g)
2C(g)
起始物质的量(mol): 3 2 0
2s末物质的量浓度(mol/L): 0.9 0.8 0.4
则①a= ,b= ;
②2S内B的反应速率= 。
(3)(2分) 1 mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式 。

(1)第三周期第ⅢA族(2分)
(2)①a=3(2分) b=1 (2分) ②0.1mol/(L·S)(2分)
(3)NO2(g) + CO(g) = CO2(g) + NO(g) △H = - 234kJ·mol-1(2分)
【解析】(1)1.5mol氢气,共转移电子是1.5mol×2=3.0mol,所以该金属原子在反应中失去3铬电子。由于离子具有氖原子的电子层结构,因此金属的原子序数为13,即为铝元素,位于第三周期第ⅢA族。
(2)根据方程式可知A、B、C的浓度变化量分别是(mol/L)0.6、0.2、0.4,所以化学计量数之比为3︰1︰2,因此a=3,b=1。B的平均反应速率是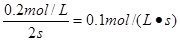 。
。
(3)根据图像可知,反应物的总能量高于生成物的总能量,所以是放热反应,反应热为134 kJ·mol-1-368 kJ·mol-1=- 234kJ·mol-1,所以反应的热化学方程式为NO2(g) + CO(g) = CO2(g) + NO(g) △H = - 234kJ·mol-1。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| 实 验 步 骤 | 解 释 或 实 验 结 论 |
| (1)称取A 9.0g,升温使其汽化,测其密度是相同条件下H2的45倍. | 试通过计算填空: (1)A的相对分子质量为: 90 90 . |
| (2)将此9.0gA在足量纯O2充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4g和13.2g. | (2)A的分子式为: C3H6O3 C3H6O3 . |
| (3)另取A 9.0g,跟足量的NaHCO3粉末反应,生成2.24LCO2(标准状况),若与足量金属钠反应则生成2.24LH2(标准状况). | (3)用结构简式表示A中含有的官能团: -COOH、-OH -COOH、-OH . |
(4)A的核磁共振氢谱如下图: |
(4)A中含有 4 4 种氢原子. |
(5)综上所述,A的结构简式  若有手性碳原子,请在结构简式上用*标出手性碳原子 | |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 滴定次数 | 待测溶液 体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 10.00 | 0.50 | 21.48 |
| 第二次 | 10.00 | 4.00 | 25.02 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| (1)称取A 9.0g,升温使其汽化,测其密度是相同条件下H2的45倍. | 试通过计算填空:(1)有机物A的相对分子质量为: 90 90 . | ||||||
| (2)将此9.0gA在足量纯O2充分燃烧,并使其产物依次通过碱石灰、无水硫酸铜粉末、足量石灰水,发现碱石灰增重14.2g,硫酸铜粉末没有变蓝,石灰水中有10.0g白色沉淀生成;向增重的碱石灰中加入足量盐酸后,产生4.48L无色无味气体(标准状况). | (2)9.0g有机物A完全燃烧时,经计算: 生成CO2共为 0.3 0.3 mol,生成的H2O 5.4 5.4 g.有机物A的分子式 C3H6O3 C3H6O3 . | ||||||
| (3)另取A 9.0g,跟足量的NaHCO3粉末反应,生成2.24LCO2(标准状况),若与足量金属钠反应则生成2.24LH2(标准状况). | (3)A的结构简式 CH3CH(OH)COOH CH3CH(OH)COOH .写出A生成B的化学方程式2CH3CH(OH)COOH
 +2H2O +2H2O2CH3CH(OH)COOH .
 +2H2O +2H2O | ||||||
| (4)有机物A可自身发生酯化反应生成六原子环的酯B. |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实 验 步 骤 | 解 释 或 实 验 结 论 |
| (1)称取A 9.0g,升温使其汽化,测其密度是相同条件下H2的45倍. | 试通过计算填空: (1)A的相对分子质量为 90 90 . |
| (2)将此9.0gA在足量纯O2充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4g和13.2g. | (2)A的分子式为 C3H6O3 C3H6O3 .] |
| (3)另取A 9.0g,跟足量的NaHCO3粉末反应,生成2.24LCO2(标准状况),若与足量金属钠反应则生成2.24LH2(标准状况). | (3)用结构简式表示A中含有的官能团 -COOH、-OH -COOH、-OH . |
(4)A的核磁共振氢谱如图: |
(4)A中含有 4 4 种氢原子.综上所述,A的结构简式为   |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com